Hvad er elementerne i gruppe 17 i den periodiske tabel?
* fluor (f)
* klor (Cl)
* brom (Br)
* jod (i)
* astatine (at)
* tennessine (ts)
Nøgleegenskaber ved halogener:
* stærkt reaktive ikke -metaller: De danner let forbindelser med andre elementer, især metaller.
* findes som diatomiske molekyler: De findes i naturen som par af atomer (f.eks. Cl₂, br₂).
* Formsalte med metaller: Halogenerne reagerer med metaller for at danne ioniske forbindelser kaldet salte.
* elektronegativ: De har en stærk tendens til at tiltrække elektroner.
* forskellige tilstande ved stuetemperatur: Fluor og klor er gasser, brom er en væske, og jod er et fast stof.
* Vigtigt i biologiske systemer: Halogener spiller afgørende roller i menneskers sundhed, såsom klor i desinfektionsmidler og jod i skjoldbruskkirtelhormonproduktionen.
Sidste artikelHvornår blev syre sort kirsebær skabt?
Næste artikelHvad sker der, når du blander Clorox med salt?
 Varme artikler
Varme artikler
-
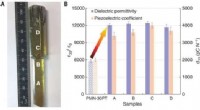 Forskere finder, at tilføjelse af sjældne jordarters element til piezoelektriske krystaller forbed…Billede og elektromekaniske egenskaber af [001]-orienterede Sm-doterede PMN-PT-krystaller. (A) Billede af Sm-PMN-PT-krystal som vokset. Sammensætningen af punkt A, B, C, og D er anført i tabel S1. (
Forskere finder, at tilføjelse af sjældne jordarters element til piezoelektriske krystaller forbed…Billede og elektromekaniske egenskaber af [001]-orienterede Sm-doterede PMN-PT-krystaller. (A) Billede af Sm-PMN-PT-krystal som vokset. Sammensætningen af punkt A, B, C, og D er anført i tabel S1. ( -
 Billeddannelse af strukturelle ændringer i katalysatorer under reaktionsbetingelserFigur (til venstre) viser den opsætning, der bruges til at fange reversible transformationer i Palladium (Pd) nanopartikler under carbonmonoxid (CO) oxidationsreaktion med operando transmission elektr
Billeddannelse af strukturelle ændringer i katalysatorer under reaktionsbetingelserFigur (til venstre) viser den opsætning, der bruges til at fange reversible transformationer i Palladium (Pd) nanopartikler under carbonmonoxid (CO) oxidationsreaktion med operando transmission elektr -
 Aske fra kraftværker forarbejdet til reagenser til vandrensningKredit:CC0 Public Domain Russiske metallurger har foreslået at opløse askeaffaldet fra termiske kraftværker med saltsyre ved højt tryk. De resulterende forbindelser kan anvendes til vandbehandling
Aske fra kraftværker forarbejdet til reagenser til vandrensningKredit:CC0 Public Domain Russiske metallurger har foreslået at opløse askeaffaldet fra termiske kraftværker med saltsyre ved højt tryk. De resulterende forbindelser kan anvendes til vandbehandling -
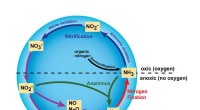 Undersøgelse af forviklingerne i nitrogenkredsløbetDenne grafik fremhæver nogle af de vigtigste reaktioner i nitrogenkredsløbet, skudt i gang med brugen af ammoniak eller NH3 , gødning. MSUs nye forskning zoomer ind på reaktioner, der involverer nit
Undersøgelse af forviklingerne i nitrogenkredsløbetDenne grafik fremhæver nogle af de vigtigste reaktioner i nitrogenkredsløbet, skudt i gang med brugen af ammoniak eller NH3 , gødning. MSUs nye forskning zoomer ind på reaktioner, der involverer nit
- Sådan fungerer elevatorer
- Hvor vigtigt er medierne i fjerntliggende områder?
- Nye MAVEN-fund afslører, hvordan Mars-atmosfæren gik tabt til rummet
- At pumpe en nanopartikel til at lasere ved lav effekt
- Elektromagnetisk bølge brugt af WiFi -routere?
- Når friskvandsprotozoa pumper ud, hvor får det energien til at gøre det?


