Er kogepunktet brint eller ilt koldere?
* Hydrogen's kogepunkt: -252,87 ° C (-423,17 ° F)
* Oxygen's kogepunkt: -182,95 ° C (-297,31 ° F)
Årsagen til denne forskel skyldes styrken af de intermolekylære kræfter mellem molekylerne.
* brint: Hydrogenmolekyler er meget små og har kun svage London -spredningskræfter mellem dem. Dette betyder, at de ikke har brug for meget energi for at overvinde disse kræfter og overgang fra en væske til en gas.
* ilt: Oxygenmolekyler er større og har stærkere London -spredningskræfter, hvilket gør dem vanskeligere at adskille og kræve en højere temperatur (højere energiindgang) for at nå deres kogepunkt.
 Varme artikler
Varme artikler
-
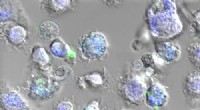 En ny slags vaccine baseret på edderkoppesilkeImmunceller, der indtog nanopartikler af edderkoppesilke (i grønt). Endosomerne - den del af cellen, hvori nanopartiklerne frigiver vaccinen - vises i blåt. Kredit:Laboratoire Bourquin – UNIGE For
En ny slags vaccine baseret på edderkoppesilkeImmunceller, der indtog nanopartikler af edderkoppesilke (i grønt). Endosomerne - den del af cellen, hvori nanopartiklerne frigiver vaccinen - vises i blåt. Kredit:Laboratoire Bourquin – UNIGE For -
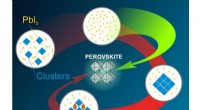 Kemikere bestemmer, hvordan man undgår biprodukter i syntesen af perovskitterRUDN -kemikere fandt ud af, hvordan man undgår biprodukter i syntesen af Perovskites Kredit:Natalia Deryugina En RUDN -professor, sammen med sine kolleger fra andre universiteter i Moskva, har b
Kemikere bestemmer, hvordan man undgår biprodukter i syntesen af perovskitterRUDN -kemikere fandt ud af, hvordan man undgår biprodukter i syntesen af Perovskites Kredit:Natalia Deryugina En RUDN -professor, sammen med sine kolleger fra andre universiteter i Moskva, har b -
 Ny software til at hjælpe med at opdage værdifulde forbindelserSammenlignende metabolomik med Metaboseek. en Metaboseek inkluderer et integreret XCMS-modul til funktionsdetektion og funktionsgruppering (med CAMERA-annotering) og accepterer funktionstabeller gener
Ny software til at hjælpe med at opdage værdifulde forbindelserSammenlignende metabolomik med Metaboseek. en Metaboseek inkluderer et integreret XCMS-modul til funktionsdetektion og funktionsgruppering (med CAMERA-annotering) og accepterer funktionstabeller gener -
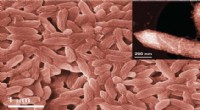 Rekruttering af bakterier til at bygge katalysatorer atom for atomForskerholdet udnyttede den jernåndende bakterie Geobacter sulfurreducens til at syntetisere enkeltatom-katalysatorer, som kan bruges til forskellige energirelaterede applikationer. Kredit:KAUST U
Rekruttering af bakterier til at bygge katalysatorer atom for atomForskerholdet udnyttede den jernåndende bakterie Geobacter sulfurreducens til at syntetisere enkeltatom-katalysatorer, som kan bruges til forskellige energirelaterede applikationer. Kredit:KAUST U
- Hvad er nitratsyre?
- Hvor mange gram i en ottendedel af en ounce?
- Find de søde pletter til genopladning af administreret akvifer
- Planetarisk kuglefræsning hjælper med at beskytte vores planet mod plastikforurening
- Hvad er formelvægten af magnesiumhydroxid, en ingrediens, der findes i antacida?
- UAE forsinker yderligere lanceringen af den første atomreaktor


