Hvad sker der, når to nitrogenatom deler elektroner?
* Triple Bond: Hvert nitrogenatom har 5 valenselektroner. For at opnå en stabil octet deler de tre par elektroner, der danner en triple Bond . Denne binding er utrolig stærk, hvilket gør nitrogengas meget ureaktiv ved stuetemperatur.
* ikke -polær kovalent binding: De delte elektroner er lige så tiltrukket af begge nitrogenatomer på grund af deres lignende elektronegativitet. Dette resulterer i en ikke -polær kovalent binding , hvilket betyder, at elektronerne deles ens.
* stabil octet: Ved at dele tre par elektroner opnår begge nitrogenatomer en stabil octet (otte valenselektroner) i deres yderste skal.
Kortfattet: Deling af elektroner mellem to nitrogenatomer resulterer i et meget stabilt, ikke -polært nitrogenmolekyle med en tredobbelt binding. Denne stærke binding gør nitrogengasinert og rigelig i atmosfæren.
 Varme artikler
Varme artikler
-
 Udvikling af enzymer til at omdanne planteaffald til bæredygtige produkterDet nyudviklede enzym. Kredit:University of Portsmouth En ny familie af enzymer er blevet konstrueret til at udføre et af de vigtigste trin i omdannelsen af planteaffald til bæredygtige og højvæ
Udvikling af enzymer til at omdanne planteaffald til bæredygtige produkterDet nyudviklede enzym. Kredit:University of Portsmouth En ny familie af enzymer er blevet konstrueret til at udføre et af de vigtigste trin i omdannelsen af planteaffald til bæredygtige og højvæ -
 Praktisk hårregenereringsteknologiKulturkar til massepræparation af hårsækkekim (ovenfor). Genereret hår på bagsiden af en mus (nedenfor). Kredit:Yokohama National University Forskere har udviklet en metode til massefremstilling
Praktisk hårregenereringsteknologiKulturkar til massepræparation af hårsækkekim (ovenfor). Genereret hår på bagsiden af en mus (nedenfor). Kredit:Yokohama National University Forskere har udviklet en metode til massefremstilling -
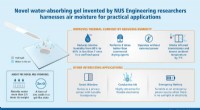 Ny hydrogel udnytter luftfugtighed til praktiske anvendelserNy vandabsorberende gel opfundet af NUS Engineering-forskere udnytter luftfugtighed til praktiske anvendelser. Kredit:National University of Singapore Høj luftfugtighed giver ubehag og får varme d
Ny hydrogel udnytter luftfugtighed til praktiske anvendelserNy vandabsorberende gel opfundet af NUS Engineering-forskere udnytter luftfugtighed til praktiske anvendelser. Kredit:National University of Singapore Høj luftfugtighed giver ubehag og får varme d -
 Forskere arbejder på at skabe mikrochipelementer i molekylær størrelseKredit:CC0 Public Domain Moderne siliciumbaserede integrerede kredsløb (ICer) har nået de praktiske grænser for miniaturisering, mens brugen af organiske stoffer potentielt kan tillade skabelsen
Forskere arbejder på at skabe mikrochipelementer i molekylær størrelseKredit:CC0 Public Domain Moderne siliciumbaserede integrerede kredsløb (ICer) har nået de praktiske grænser for miniaturisering, mens brugen af organiske stoffer potentielt kan tillade skabelsen
- Hvad er de to typer faktorer, som et økosystem har?
- Sådan beregnes grundlæggende frekvens
- Quantum tilfældigt tal generator sætter benchmark for størrelse, ydeevne
- Undersøgelse afslører, at opfattet kønsbias mod kvinder er en dominerende faktor i kollegiets hov…
- Er der nogen videnskabelige ord i sjette klasse, der starter med Y?
- Hvorfor har vi brug for mere end bare data for at skabe etiske førerløse biler


