Hvad er ligheder mellem ioniske kovalente og metalliske bindinger?
1. De involverer alle interaktion mellem valenselektroner:
* ionisk: Elektroner overføres fra et atom til et andet, danner ioner med modsatte ladninger, der tiltrækker hinanden.
* kovalent: Elektroner deles mellem atomer.
* Metallic: Valenselektroner er delokaliserede og frie til at bevæge sig gennem hele metalgitteret.
2. De bidrager alle til dannelsen af stabile forbindelser:
* ionisk: Den elektrostatiske tiltrækning mellem modsat ladede ioner fører til en stabil forbindelse.
* kovalent: Deling af elektroner skaber en stabil elektronkonfiguration for hvert atom, hvilket resulterer i et stabilt molekyle.
* Metallic: Den stærke tiltrækning mellem metalkationerne og de delokaliserede elektroner resulterer i en stabil metallisk krystal.
3. De involverer alle elektrostatiske interaktioner:
* ionisk: Direkte elektrostatisk tiltrækning mellem ioner.
* kovalent: Elektrostatisk tiltrækning mellem de delte elektroner og de positivt ladede kerner.
* Metallic: Elektrostatisk tiltrækning mellem de positivt ladede metalkationer og det negativt ladede hav af delokaliserede elektroner.
4. De påvirker alle de fysiske egenskaber ved materialer:
* ionisk: Danner ofte hårde, sprøde krystaller med høje smeltepunkter og god elektrisk ledningsevne, når de blev opløst i vand.
* kovalent: Kan danne faste stoffer, væsker eller gasser med forskellige smeltepunkter og elektrisk ledningsevne afhængigt af typen af kovalent binding.
* Metallic: Danner typisk stærke, formbare og duktile faste stoffer, der er gode ledere af varme og elektricitet.
Nøgleforskelle
Mens disse ligheder findes, ligger de vigtigste forskelle i form af elektrondeling eller overførsel, og de resulterende egenskaber for de dannede forbindelser.
* ionisk: Komplet elektronoverførsel, stærk elektrostatisk attraktion, højt smeltepunkt, sprødt, ofte opløseligt i vand.
* kovalent: Elektrondeling, stærke bindinger, forskellige smeltepunkter, kan være gasser, væsker eller faste stoffer, dårlig elektrisk ledningsevne.
* Metallic: Delokaliserede elektroner, stærke metalliske bindinger, højt smeltepunkt, formbare, duktile, gode elektriske og termiske ledningsevne.
Det er vigtigt at huske, at disse kategorier repræsenterer ideelle tilfælde, og reelle materialer kan udvise karakteristika for mere end en type binding.
 Varme artikler
Varme artikler
-
 Ny medicinsk billedbehandlingstilgang åbner mulighed for forbedrede diagnoser og interventionerKredit:CC0 Public Domain Forskere fra Helmholtz Zentrum München og University of California, Los Angeles (UCLA), i fællesskab udviklet nye billeddannelsesværktøjer for at muliggøre ikke-invasiv bi
Ny medicinsk billedbehandlingstilgang åbner mulighed for forbedrede diagnoser og interventionerKredit:CC0 Public Domain Forskere fra Helmholtz Zentrum München og University of California, Los Angeles (UCLA), i fællesskab udviklet nye billeddannelsesværktøjer for at muliggøre ikke-invasiv bi -
 Forskere afslører kunsten at trykke ekstremt hårdt stål fejlfritMartensit stålpulver brugt til 3D-print. Indsat viser en zoomet visning af stålpulveret. Kredit:Raiyan Seede/Texas A&M University College of Engineering I årtusinder, metallurger har omhyggeligt j
Forskere afslører kunsten at trykke ekstremt hårdt stål fejlfritMartensit stålpulver brugt til 3D-print. Indsat viser en zoomet visning af stålpulveret. Kredit:Raiyan Seede/Texas A&M University College of Engineering I årtusinder, metallurger har omhyggeligt j -
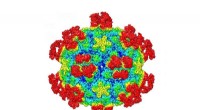 Ny mekanisme til at ødelægge vira kan føre til fremtidige behandlingerDer vises et overfladebillede af en almindelig forkølelsesvirus, når den er kompleks med det antigenbindende fragment af et neutraliserende antistof. Farverne svarer til overfladens afstand fra virusc
Ny mekanisme til at ødelægge vira kan føre til fremtidige behandlingerDer vises et overfladebillede af en almindelig forkølelsesvirus, når den er kompleks med det antigenbindende fragment af et neutraliserende antistof. Farverne svarer til overfladens afstand fra virusc -
 Forskere kontrollerer de elektriske egenskaber af optiske hukommelsesenhederKredit: Journal of Materials Chemistry C (2019). DOI:10.1039/c9tc01273g En gruppe forskere fra Skoltech, Instituttet for problemer med kemisk fysik i RAS, og N.D. Zelinsky Institute of Organic Ch
Forskere kontrollerer de elektriske egenskaber af optiske hukommelsesenhederKredit: Journal of Materials Chemistry C (2019). DOI:10.1039/c9tc01273g En gruppe forskere fra Skoltech, Instituttet for problemer med kemisk fysik i RAS, og N.D. Zelinsky Institute of Organic Ch
- Elektronacceleratorer afslører de radikale hemmeligheder ved antioxidanter
- Flyrejser og klima:En potentiel ny feedback?
- Mikrober under Grønlands is kan være et eksempel på, hvad forskere finder Mars' overflade
- Hvordan man laver saltkrystaller derhjemme
- Solvatiseringsdrevet elektrokemisk aktivering
- Erfaringer fra Sierra Leones Ebola-pandemi om virkningen af skolelukninger på piger


