Hvad er to sekundære faktorer, der påvirker opløst diffusion?
1. Opløsningsmidlets art:
* Viskositet: Et mere tyktflydende opløsningsmiddel (som honning) vil hindre opløst bevægelse og bremse diffusion. Dette skyldes, at molekyler skal skubbe gennem et tættere, mere resistent medium.
* Polaritet: Opløsnings- og opløsningsmiddelpolaritet spiller en vigtig rolle. Polære opløste stoffer (som sukker) opløses godt i polære opløsningsmidler (som vand), mens ikke -polære opløste stoffer (som fedt) opløses godt i ikke -polære opløsningsmidler (som olie). Dette skyldes de attraktive kræfter mellem lignende molekyler. Hvis opløsningen og opløsningsmidlet har forskellige polariteter, vil diffusion være markant langsommere.
2. Tilstedeværelsen af andre opløste stoffer:
* trængsel: Hvis løsningen allerede er overfyldt med andre opløste stoffer, er der mindre plads til, at målløsten kan bevæge sig. Dette kan føre til langsommere diffusion.
* interaktioner: Tilstedeværelsen af andre opløste stoffer kan interagere med målopløsningen, enten tiltrække eller afvise det. Disse interaktioner kan ændre diffusionshastigheden. For eksempel kan elektrolytter (ladede ioner) interagere med hinanden og påvirke deres bevægelse.
Det er vigtigt at huske, at dette er sekundære faktorer, hvilket betyder, at de normalt er mindre signifikante end koncentrationsgradient og temperatur. De kan dog stadig have en mærkbar indflydelse på den samlede diffusionshastighed under visse omstændigheder.
Sidste artikelHvad er massen på 15 mols wolfram?
Næste artikelPåvirker densiteten af en væske dens dråbeform?
 Varme artikler
Varme artikler
-
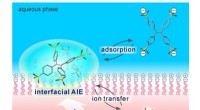 Belysning af vejen til selektiv membranbilleddannelseVandopløselige tetraphenylethen (TPE) derivater, der bærer anioniske grupper, udviser aggregeringsinduceret emission (AIE) adfærd specifikt ved væske-væske-grænseflader. Interfacial AIE-proces reagere
Belysning af vejen til selektiv membranbilleddannelseVandopløselige tetraphenylethen (TPE) derivater, der bærer anioniske grupper, udviser aggregeringsinduceret emission (AIE) adfærd specifikt ved væske-væske-grænseflader. Interfacial AIE-proces reagere -
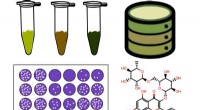 Et stof, der findes i brunkul, kan hjælpe med at bekæmpe viraAntiviral aktivitet af ti humusstofprøver (HS) blev vurderet mod flåtbåren encephalitisvirus reproduktion. For at afsløre mulige aktive komponenter i HS -prøver blev der søgt efter FTICR MS -data i Ch
Et stof, der findes i brunkul, kan hjælpe med at bekæmpe viraAntiviral aktivitet af ti humusstofprøver (HS) blev vurderet mod flåtbåren encephalitisvirus reproduktion. For at afsløre mulige aktive komponenter i HS -prøver blev der søgt efter FTICR MS -data i Ch -
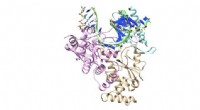 Trækker stikket på coronavirus kopimaskineAntiviralt lægemiddel remdesivir udgør hovedlinjen i FDA-godkendt terapeutisk forsvar mod COVID-19-virussen. Forskere ved University of North Texas bruger Frontera-supercomputeren til at modellere, hv
Trækker stikket på coronavirus kopimaskineAntiviralt lægemiddel remdesivir udgør hovedlinjen i FDA-godkendt terapeutisk forsvar mod COVID-19-virussen. Forskere ved University of North Texas bruger Frontera-supercomputeren til at modellere, hv -
 Video:Hortensiaer og videnskaben om gør-oversKredit:The American Chemical Society I en tidligere video, Reactions-holdet forsøgte at demonstrere den farveskiftende videnskab om hortensia ved at bruge aluminiumcitrat til at forsøge at forvand
Video:Hortensiaer og videnskaben om gør-oversKredit:The American Chemical Society I en tidligere video, Reactions-holdet forsøgte at demonstrere den farveskiftende videnskab om hortensia ved at bruge aluminiumcitrat til at forsøge at forvand
- Billede:Hubble finder Medusa på himlen
- Flerfasebuffring med ammoniak forklarer en bred vifte af atmosfærisk aerosolsurhed
- Hvilket hovedvæv beklæder kroppens hulrum og dækker den ydre overflade?
- Omdannelse af LBM til Gallons
- Forskere peger på, hvordan detektion af sociale signaler kan have påvirket vi ser farver
- Uro i træg elektroner eksistens


