Hvad er når molekyler tiltrækkes af hinanden, men ikke bestilles?
* attraktion: Væsker har stærke nok intermolekylære kræfter (som hydrogenbindinger, dipol-dipolinteraktioner eller London-spredningskræfter) til at holde molekylerne sammen.
* Manglende orden: I modsætning til faste stoffer, hvor molekyler er stift arrangeret i et krystalgitter, har væsker mindre orden. Deres molekyler bevæger sig konstant og støder på hinanden, hvilket resulterer i en mere flydende og mindre organiseret struktur.
her er en simpel analogi: Forestil dig et overfyldt dansegulv. Folk er tæt på hinanden (tiltrækning), men de bevæger sig alle frit og støder på hinanden (manglende orden). Det er ligesom hvordan molekyler opfører sig i en væske.
Sidste artikelAtomer tiltrækkes af hinanden, når de har hvad?
Næste artikelHvordan kan alkalier fjerne fedt og olie?
 Varme artikler
Varme artikler
-
 En venligere måde at håndtere nitratforurening påKredit:CC0 Public Domain At lære af naturen, forskere fra Center for Sustainable Resource Science i Japan og Korean Basic Science Institute (KBSI) har fundet en katalysator, der effektivt omdanner
En venligere måde at håndtere nitratforurening påKredit:CC0 Public Domain At lære af naturen, forskere fra Center for Sustainable Resource Science i Japan og Korean Basic Science Institute (KBSI) har fundet en katalysator, der effektivt omdanner -
 Nye materialer til at hjælpe med at stoppe lithium-ion-batteri, eksplosioner og forbedrer batteriet…Dette billede viser en høj ionisk ledende og fleksibel polymer komposit elektrolytfilm til lithium-ion batterier. Kredit:Purdue University Fra biler og fly til bærbare computere og e-cykler, lithi
Nye materialer til at hjælpe med at stoppe lithium-ion-batteri, eksplosioner og forbedrer batteriet…Dette billede viser en høj ionisk ledende og fleksibel polymer komposit elektrolytfilm til lithium-ion batterier. Kredit:Purdue University Fra biler og fly til bærbare computere og e-cykler, lithi -
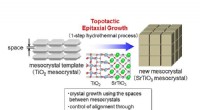 Fotokatalysator gør brintproduktion 10 gange mere effektivSyntese af SrTiOmeso-krystaller ved topotaktisk epitaksial vækst. Kredit:Kobe University Brint er en alternativ energikilde, der kan produceres fra vedvarende kilder til sollys og vand. En gruppe
Fotokatalysator gør brintproduktion 10 gange mere effektivSyntese af SrTiOmeso-krystaller ved topotaktisk epitaksial vækst. Kredit:Kobe University Brint er en alternativ energikilde, der kan produceres fra vedvarende kilder til sollys og vand. En gruppe -
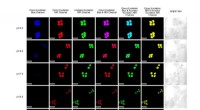 Gør en god ting bedre:En syretest, der ikke vil drukne i vandMichigan Tech kemikere dyrkede levende celler under forskellige pH-forhold, behandlede dem med et nyt fluorescerende cyaninfarvestof og fangede deres billeder under forskellige lysfrekvenser, både syn
Gør en god ting bedre:En syretest, der ikke vil drukne i vandMichigan Tech kemikere dyrkede levende celler under forskellige pH-forhold, behandlede dem med et nyt fluorescerende cyaninfarvestof og fangede deres billeder under forskellige lysfrekvenser, både syn
- Stærkeste typer af lim
- Forskere løser mysteriet med farverige nanorør til lænestole
- Forskere når det ultimative mål:Kontrol af chiralitet i carbon nanorør
- Lader de blade hobe sig op? Ny forskning viser, at bladaffald indeholder vedvarende frie radikaler
- Ingeniør opdager mægtig kraft i opfindelsen med lille solenergi
- Hvordan elektronisk hud kunne hjælpe mennesker med handicap


