Hvorfor forbrænding af metal betyder at have reaktion med ilt?
* Oxidation: Dette er en kemisk proces, hvor et stof mister elektroner.
* Metaller: Metaller har en tendens til at have løst holdt elektroner i deres ydre skaller. Dette gør dem let tilgængelige for at gå tabt under kemiske reaktioner.
* ilt: Oxygen er et meget elektronegativt element, hvilket betyder, at det stærkt tiltrækker elektroner.
Når et metal brænder:
1. varme: Varmen fra brændende proces giver den energi, der er nødvendig for at starte reaktionen.
2. ilt: Metallet reagerer med ilt i luften.
3. Elektronoverførsel: Metalatomerne mister elektroner (oxidation), og iltatomerne får elektroner. Dette danner metaloxid, som normalt er et fast stof.
4. Energifrigivelse: Denne kemiske reaktion frigiver energi i form af lys og varme, som vi opfatter som metallet "brændende".
Eksempel:
* jernforbrænding: Når jernforbrændinger (rustning er en langsom form for forbrænding), reagerer det med ilt for at danne jernoxid (rust). Den kemiske ligning er:
* 4Fe + 3o₂ → 2Fe₂o₃
Nøglepunkter:
* Brændende metaller er ikke det samme som brændende brændstoffer som træ eller gas. Brændstoffer frigiver energi fra kemiske bindinger, mens metaller frigiver energi gennem tab af elektroner.
* Ikke alle metaller brænder let. Nogle metaller, som guld og platin, er meget modstandsdygtige over for oxidation.
Fortæl mig, hvis du gerne vil have flere detaljer om oxidationsprocessen eller den specifikke forbrænding af forskellige metaller!
Sidste artikelHvor i dine makromolekyler findes nitrogen og fosfater?
Næste artikelHvad er det mest sprøde stof?
 Varme artikler
Varme artikler
-
 Usædvanligt sukker fra cyanobakterier virker som naturligt herbicidCyanobakterier i laboratoriet:Den nye aktive ingrediens blev isoleret fra kulturer af ferskvandscyanobakterien Synechococcus elongatus. Kredit:Klaus Brilisauer Forskere ved universitetet i Tübinge
Usædvanligt sukker fra cyanobakterier virker som naturligt herbicidCyanobakterier i laboratoriet:Den nye aktive ingrediens blev isoleret fra kulturer af ferskvandscyanobakterien Synechococcus elongatus. Kredit:Klaus Brilisauer Forskere ved universitetet i Tübinge -
 Forskere udvikler guldkompleksbundne ferrocenylphosphiner som potente malariamidlerGuldkonjugerede ferrocinylphosphiner, der hæmmer fordøjelsesvakuolefunktionen af malariaparasitten, Plasmodium falciparum. Kredit:SUTD Et team af forskere fra Singapore University of Technology
Forskere udvikler guldkompleksbundne ferrocenylphosphiner som potente malariamidlerGuldkonjugerede ferrocinylphosphiner, der hæmmer fordøjelsesvakuolefunktionen af malariaparasitten, Plasmodium falciparum. Kredit:SUTD Et team af forskere fra Singapore University of Technology -
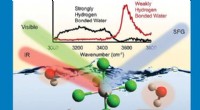 Unik grænseflade og uventet adfærd hjælper med at forklare, hvordan tungmetaller virkerForskere identificerede tre forskellige typer vandmolekyler, der omgiver en tung, anionisk metalchloridkompleks (nederst) ved brug af spektroskopi (øverst) ved en luft/vand-grænseflade. Hver type vand
Unik grænseflade og uventet adfærd hjælper med at forklare, hvordan tungmetaller virkerForskere identificerede tre forskellige typer vandmolekyler, der omgiver en tung, anionisk metalchloridkompleks (nederst) ved brug af spektroskopi (øverst) ved en luft/vand-grænseflade. Hver type vand -
 Ny katalysator gør styrenfremstilling billigere, grønnereKredit:North Carolina State University Kemiingeniørforskere har udviklet en ny katalysator, der markant øger udbyttet i styrenfremstilling, samtidig med at energiforbruget og drivhusgasemissionern
Ny katalysator gør styrenfremstilling billigere, grønnereKredit:North Carolina State University Kemiingeniørforskere har udviklet en ny katalysator, der markant øger udbyttet i styrenfremstilling, samtidig med at energiforbruget og drivhusgasemissionern
- Atomisk opfattelse af naturens fantastiske molekylære maskiner på arbejde
- De dødeligste vulkanudbrud i de sidste 25 år
- NASA-billeder afslører Neoguri nu ekstra-tropisk
- Australiens katastrofale fisk dør:Hvad er der sket siden 2019
- Tibets eksilmuslimer viser forviklinger af kultur, identitet for flygtninge
- Kelp, maddiker og mykoprotein blandt fremtidige fødevarer, der skal masseopdrættes for at bekæmpe…


