Hvad er de mest aktive familiemetaller?
Hvis du spørger om den mest reaktive gruppe af metaller, det ville være alkali -metaller (Gruppe 1). Disse metaller, herunder lithium (Li), natrium (NA), kalium (K), rubidium (RB), cesium (CS) og francium (FR), er meget reaktive på grund af deres enkelt valenselektron, som de let mister for at danne positive ioner.
Her er grunden til, at de betragtes som de mest reaktive:
* lav ioniseringsenergi: Det kræver meget lidt energi at fjerne deres enkelt valenselektron.
* stor atomradius: Deres yderste elektron er langt fra kernen og holdes svagt.
* Lav elektronegativitet: De mister let elektroner for at blive kationer, hvilket gør dem til gode reduktionsmidler.
Vigtig note: ALKALI -METALERS Reaktivitet øges, når du bevæger dig ned ad gruppen. Dette betyder, at cæsium er den mest reaktive af alkalimetaller, efterfulgt af Francium. Imidlertid er Francium et radioaktivt element og meget sjældent, så cæsium betragtes som det mest reaktive element i denne gruppe.
Sidste artikelHvad er P91 -materiale?
Næste artikelHvilket stof gør koral hårdt?
 Varme artikler
Varme artikler
-
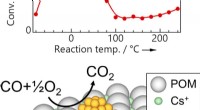 Ultraeffektiv fjernelse af kulilte ved hjælp af guld nanopartikler på en molekylær støtteNy katalysator bestående af guldnanopartikler understøttet på et Keggin-type polyoxometalat (POM) med et cæsiumsalt. Strukturen viste høj aktivitet og stabilitet for CO-oxidation; spormængder af vand
Ultraeffektiv fjernelse af kulilte ved hjælp af guld nanopartikler på en molekylær støtteNy katalysator bestående af guldnanopartikler understøttet på et Keggin-type polyoxometalat (POM) med et cæsiumsalt. Strukturen viste høj aktivitet og stabilitet for CO-oxidation; spormængder af vand -
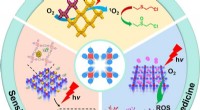 Seneste fremskridt i udviklingen af foto- og elektroaktive hydrogenbundne organiske rammerI midten kan det ses, at HOFer med optoelektroniske egenskaber har en bred vifte af anvendelser inden for katalyse, sansning og biomedicin. Kredit:©Science China Press HOFer er en klasse af krystal
Seneste fremskridt i udviklingen af foto- og elektroaktive hydrogenbundne organiske rammerI midten kan det ses, at HOFer med optoelektroniske egenskaber har en bred vifte af anvendelser inden for katalyse, sansning og biomedicin. Kredit:©Science China Press HOFer er en klasse af krystal -
 Hvordan reducerer man drivhusgasser? Tips fra en metanædende mikrobeMetan-spisende bakterier findes i ekstreme miljøer såsom aktive geotermiske varme kilder. Kredit:Inger Eriksen/Shutterstock Forskere har bestemt strukturen af et unikt enzym, produceret af en ar
Hvordan reducerer man drivhusgasser? Tips fra en metanædende mikrobeMetan-spisende bakterier findes i ekstreme miljøer såsom aktive geotermiske varme kilder. Kredit:Inger Eriksen/Shutterstock Forskere har bestemt strukturen af et unikt enzym, produceret af en ar -
 Flydende metaller de hemmelige ingredienser til at rense miljøetKredit:CC0 Public Domain Glem laboratoriet, stoffer, der kan løse miljøproblemer ved at opfange kuldioxid, dekontaminering af vand og oprensning af forurenende stoffer kan nemt skabes i et køkken,
Flydende metaller de hemmelige ingredienser til at rense miljøetKredit:CC0 Public Domain Glem laboratoriet, stoffer, der kan løse miljøproblemer ved at opfange kuldioxid, dekontaminering af vand og oprensning af forurenende stoffer kan nemt skabes i et køkken,
- Hvordan kunstige intelligenssystemer kunne true demokratiet
- Når kontinentalplader trækker fra hinanden danner de dette?
- Forskere udviklede enkeltcelleniveau sorteringsteknologi ved hjælp af lydbølger
- Hvilken ligning bruges til at beregne mængden af brugt elektrisk energi?
- Har hjerneceller et lipid bilayer?
- Hvordan laver man ilt i lille alkymi?


