Hvordan bliver et atom af bor stabilt?
Borons elektroniske konfiguration
* Bor har et atomnummer på 5, hvilket betyder, at det har 5 protoner og 5 elektroner.
* Dens elektronkonfiguration er 1S² 2S² 2P¹. Dette betyder, at det har 3 elektroner i sin yderste skal (den 2. skal).
Octet -reglen
* Atomer stræber efter stabilitet ved at opnå en fuld ydre skal af elektroner. Dette er kendt som Octet -reglen, som generelt betyder at have 8 elektroner i deres yderste skal.
* Der er dog undtagelser, og bor er en af dem.
Borons stabilitet
* Bor opnår stabilitet ved at danne kovalente obligationer med andre atomer.
* Ved at dele sin ene elektron i 2p orbital kan bor opnå en stabil konfiguration med 4 elektroner i dens ydre skal (2 fra 2'erne orbital og 2 fra de delte elektroner).
* Dette er kendt som "ufuldstændig oktet" Undtagelse fra Octet -reglen.
Eksempler på bores stabilitet
* bortrifluorid (BF3): Boren deler sine tre valenselektroner med tre fluoratomer og danner tre kovalente bindinger. Dette giver bor i alt seks elektroner i sin ydre skal.
* Borane (BH3): Bor danner tre kovalente bindinger med hydrogenatomer og opnår en lignende stabil konfiguration.
Kortfattet:
Bor bliver stabil ved at danne kovalente bindinger med andre atomer og dele dens elektroner for at opnå en stabil elektronkonfiguration, selvom den ikke har en fuld oktet.
 Varme artikler
Varme artikler
-
 Forstå, hvad der gør sort pigment sortKredit:CC0 Public Domain Forskere har for første gang ublandet det sorte pigment, der farver vores hud og giver bananerne deres pletter. Forskere ved Ohio State University udførte arbejdet med eu
Forstå, hvad der gør sort pigment sortKredit:CC0 Public Domain Forskere har for første gang ublandet det sorte pigment, der farver vores hud og giver bananerne deres pletter. Forskere ved Ohio State University udførte arbejdet med eu -
 Forskere laver verdens mindste sammenkædede kæderForskere opdagede en måde at fremstille små sammenlåsende kæder (højre, med kemiske formler til venstre) med sløjfer hver kun en nanometer på tværs. Kredit:Peter Allen I årtier, videnskabsmænd har
Forskere laver verdens mindste sammenkædede kæderForskere opdagede en måde at fremstille små sammenlåsende kæder (højre, med kemiske formler til venstre) med sløjfer hver kun en nanometer på tværs. Kredit:Peter Allen I årtier, videnskabsmænd har -
 Fosforbaserede kompositter som anodematerialer til kalium-ion-batterierSkematisk illustration af de fosforbaserede kompositter som anodematerialer til KIBer. Kredit:WU Ying og HUANG Haibo Prof. WU Zhongshuai fra Dalian Institute of Chemical Physics (DICP) ved det kin
Fosforbaserede kompositter som anodematerialer til kalium-ion-batterierSkematisk illustration af de fosforbaserede kompositter som anodematerialer til KIBer. Kredit:WU Ying og HUANG Haibo Prof. WU Zhongshuai fra Dalian Institute of Chemical Physics (DICP) ved det kin -
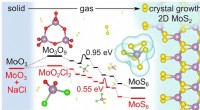 Undersøgelsesdetaljer, hvorfor 2D-molybdændisulfiddannelse får et hastighedsboost fra saltAlmindelig salt (NaCl) fungerer som et mellemled i den kemiske dampaflejringsvækst af 2D molybdændisulfid, hvilket fremskynder processen med dets skabelse. Materialeteoretikere ved Rice University opd
Undersøgelsesdetaljer, hvorfor 2D-molybdændisulfiddannelse får et hastighedsboost fra saltAlmindelig salt (NaCl) fungerer som et mellemled i den kemiske dampaflejringsvækst af 2D molybdændisulfid, hvilket fremskynder processen med dets skabelse. Materialeteoretikere ved Rice University opd
- FORGÅDE OXIDATION OG REDUKTION SAMTIDIGT?
- Gør begrænset underjordisk vandopbevaring planter mindre modtagelige for tørke?
- Fluorescerende polymer registrerer spor af eksplosive enheder
- Discovery fjerner pres fra blodmålinger
- Hvad er et eksempel på partikler?
- Et robust AI-centreret indendørs positioneringssystem


