Hvordan er egenskaben af overfladespænding relateret til struktur et vandmolekyle?
vandmolekylstruktur:
* Polaritet: Vandmolekyler er bøjede og har en polær struktur. Oxygenatomet er mere elektronegativt, tiltrækker de delte elektroner og udvikler en delvis negativ ladning (Δ-), mens de to hydrogenatomer har delvis positive ladninger (Δ+).
* Hydrogenbinding: Denne polaritet giver mulighed for, at stærke brintbindinger dannes mellem vandmolekyler. Det positivt ladede brint af et vandmolekyle tiltrækkes af den negativt ladede ilt af en anden.
Hvordan struktur fører til overfladespænding:
1. sammenhængende kræfter: Hydrogenbindingerne mellem vandmolekyler skaber stærke sammenhængende kræfter, hvilket betyder, at de tiltrækker hinanden stærkt.
2. overfladelag: På overfladen af en vandlegeme er vandmolekyler kun omgivet af andre vandmolekyler på den ene side. Dette betyder, at de oplever et stærkere indadgående træk fra de sammenhængende kræfter i molekylerne under dem end de svagere kræfter fra luftmolekylerne ovenfor.
3. minimering af overfladeareal: For at minimere denne ubalance danner vandmolekyler ved overfladen et stramt, sammenhængende lag, hvilket skaber en høj overfladespænding. Denne spænding fungerer som en usynlig elastisk membran, modstå forstyrrelse og tillader genstande som insekter at gå på vand.
Kortfattet:
Den unikke struktur af vandmolekyler med deres polaritet og evne til at danne stærke brintbindinger er ansvarlig for de stærke sammenhængende kræfter, der fører til høj overfladespænding. Denne egenskab er afgørende for mange biologiske og fysiske processer, herunder vandbevægelse gennem planter, dannelsen af regndråber og nogle dyrs evne til at gå på vand.
Sidste artikelHvad er de grundlæggende videnskabelige processer?
Næste artikelHvordan skifter du en gas til væske?
 Varme artikler
Varme artikler
-
 SwissFEL gør proteinstrukturer synligeMichael Hennig (til venstre) og Karol Nass på forsøgsstationen i SwissFEL, hvor deres pilotforsøg blev udført. Kredit:Paul Scherrer Institute/Mahir Dzambegovic Til udvikling af nye lægemidler, præ
SwissFEL gør proteinstrukturer synligeMichael Hennig (til venstre) og Karol Nass på forsøgsstationen i SwissFEL, hvor deres pilotforsøg blev udført. Kredit:Paul Scherrer Institute/Mahir Dzambegovic Til udvikling af nye lægemidler, præ -
 Et forskerhold udvikler biotransistorer, der er i stand til at detektere de mindste signalerKredit:CC0 Public Domain En af de tests, som næsten hver patient skal stå over for før en operation eller anden sundhedsintervention, er et elektrokardiogram. For at udføre denne screening, læger
Et forskerhold udvikler biotransistorer, der er i stand til at detektere de mindste signalerKredit:CC0 Public Domain En af de tests, som næsten hver patient skal stå over for før en operation eller anden sundhedsintervention, er et elektrokardiogram. For at udføre denne screening, læger -
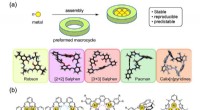 Metalliske komplekser lavet af cykliske molekylerModerne makrocykler brugt til syntese af diskrete polymetalliske komplekser:(a) koncept, (b) kemiske strukturer af repræsentative polymetalliske komplekser. Kredit:Kanazawa University I polymetall
Metalliske komplekser lavet af cykliske molekylerModerne makrocykler brugt til syntese af diskrete polymetalliske komplekser:(a) koncept, (b) kemiske strukturer af repræsentative polymetalliske komplekser. Kredit:Kanazawa University I polymetall -
 Enhed på størrelse med mønt registrerer mæslingevirus i spytKredit:Unsplash/CC0 Public Domain Mæslinger er en af de mest smitsomme luftbårne vira på verdensplan. En billig og effektiv vaccine er tilgængelig, men mæslinger er almindelig i udviklingslande,
Enhed på størrelse med mønt registrerer mæslingevirus i spytKredit:Unsplash/CC0 Public Domain Mæslinger er en af de mest smitsomme luftbårne vira på verdensplan. En billig og effektiv vaccine er tilgængelig, men mæslinger er almindelig i udviklingslande,
- Hvilken af disse er defineret som indtryk, der er tilbage i klipper af levende ting, der døde i l…
- Cellernes dans:En menuet eller en mosh?
- Hvilke geologiske træk er skabt af divergerende grænser?
- Forskere opdager, hvad vampyrblæksprutter spiser:Det er ikke du tror (Opdatering)
- Naturlig solafskærmning til trægulve og møbler
- Blæser et klimaanlæg varme eller kold luft ud?


