Molekyler pakkes tættere ind?
Her er hvorfor:
* faste stoffer: I faste stoffer holdes molekyler sammen af stærke intermolekylære kræfter, hvilket får dem til at vibrere i faste positioner. Dette skaber en stiv struktur med meget lidt plads mellem molekyler.
* væsker: I væsker har molekyler mere frihed til at bevæge sig rundt end i faste stoffer. De er stadig tæt på hinanden, men de kan glide forbi hinanden. Dette betyder, at der er mere plads mellem dem end i faste stoffer.
* Gasser: I gasser er molekyler meget langt fra hinanden og bevæger sig frit. De kolliderer med hinanden og væggene i deres beholder, men de har ikke stærke attraktive kræfter, der holder dem sammen. Dette resulterer i meget mere plads mellem gasmolekyler end i væsker eller faste stoffer.
Fortæl mig, hvis du gerne vil lære mere om materiens tilstande!
Sidste artikelHvordan er partikler arrangeret i et fast metal?
Næste artikel4 hovedklasser af kulstofforbindelser?
 Varme artikler
Varme artikler
-
 Forskere udvikler potentielt billige, lavemissionsteknologi, der kan omdanne metan uden at danne CO2Brintproduktion med en Ni-Bi smeltet katalysator Kredit:Brian Long Mens vi arbejder hen imod mere bæredygtige måder at styrke vores livsstil på, der er en søgen efter at bygge bro mellem de kuldio
Forskere udvikler potentielt billige, lavemissionsteknologi, der kan omdanne metan uden at danne CO2Brintproduktion med en Ni-Bi smeltet katalysator Kredit:Brian Long Mens vi arbejder hen imod mere bæredygtige måder at styrke vores livsstil på, der er en søgen efter at bygge bro mellem de kuldio -
 Forskere udvikler billige, høj strømtæthed vanadium flow batteri stakNy generation af vanadiumflow-batteristabelteknologi tilbyder lave omkostninger og høj effekttæthed. Kredit:SHI Dingqin Udviklingen af vedvarende energikilder såsom vind- og solenergi er begræns
Forskere udvikler billige, høj strømtæthed vanadium flow batteri stakNy generation af vanadiumflow-batteristabelteknologi tilbyder lave omkostninger og høj effekttæthed. Kredit:SHI Dingqin Udviklingen af vedvarende energikilder såsom vind- og solenergi er begræns -
 Forskere laver verdens mindste sammenkædede kæderForskere opdagede en måde at fremstille små sammenlåsende kæder (højre, med kemiske formler til venstre) med sløjfer hver kun en nanometer på tværs. Kredit:Peter Allen I årtier, videnskabsmænd har
Forskere laver verdens mindste sammenkædede kæderForskere opdagede en måde at fremstille små sammenlåsende kæder (højre, med kemiske formler til venstre) med sløjfer hver kun en nanometer på tværs. Kredit:Peter Allen I årtier, videnskabsmænd har -
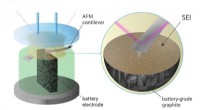 Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p
Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p
- Hvilken planet har det stærkeste træk?
- Vælger du en mobiltelefon, receptpligtig medicin eller ny bil? Læs dette først
- Hvorfor er lavvandede søer udsat for eutrofiering?
- Rapport bygger rammer for digital politisk etik i 2020
- Hvad gør astronauter til underholdning i rummet?
- Spintronics:Hvordan en atomtynd isolator hjælper med at transportere spins


