Bliver elementer mere metalliske, når du går ned i grupper?
* stigende atomradius: Når du bevæger dig ned ad en gruppe, øges antallet af elektronskaller. Dette fører til en større atomradius, hvilket betyder, at de yderste elektroner er længere væk fra kernen.
* Faldende ioniseringsenergi: De yderste elektroner holdes mindre tæt af kernen på grund af den øgede afstand. Dette resulterer i lavere ioniseringsenergi, hvilket gør det lettere at fjerne elektroner og danne positive ioner, et nøgleegenskab for metaller.
* Faldende elektronegativitet: Elektronegativitet, et atomens tendens til at tiltrække elektroner, falder, når du går ned i en gruppe. Dette betyder, at metaller, der er lavere i en gruppe, er mindre tilbøjelige til at tiltrække elektroner og mere tilbøjelige til at miste dem, hvilket yderligere bidrager til deres metalliske karakter.
Undtagelser:
Mens tendensen gælder for de fleste elementer, er der nogle undtagelser, især i de nedre grupper. For eksempel:
* gruppe 14: Tin (SN) og bly (PB) viser en mere metallisk karakter sammenlignet med kulstof og silicium.
* gruppe 15: Bismuth (BI) viser metalliske egenskaber på trods af at være i den samme gruppe som ikke -metaler som nitrogen og fosfor.
Husk: Den periodiske tabel er en smuk repræsentation af tendenser, men det er altid vigtigt at overveje individuelle elementer og deres unikke egenskaber.
Sidste artikelHvad er en partikel med negativ ændring?
Næste artikelGiv mere eksempel på et formbart materiale?
 Varme artikler
Varme artikler
-
 Forskere skaber titaniumdele ved hjælp af additivteknologierProf. M. Samodurova, Leder af SUSU International Laboratory of Mechanics, Laserprocesser og digitale produktionsteknologier. Kredit:SUSU Fremstilling af produkter af titanium og dets legeringer ve
Forskere skaber titaniumdele ved hjælp af additivteknologierProf. M. Samodurova, Leder af SUSU International Laboratory of Mechanics, Laserprocesser og digitale produktionsteknologier. Kredit:SUSU Fremstilling af produkter af titanium og dets legeringer ve -
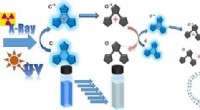 Usynlige røntgenstråler bliver blåDe farlige stråler som ultraviolet og røntgenoxidativ udløser den farveskiftende kaskade af nye farvestoffer 1000 gange. Kredit:Tsuyoshi Kawai Et nyt reaktionssystem kan registrere røntgenstråler
Usynlige røntgenstråler bliver blåDe farlige stråler som ultraviolet og røntgenoxidativ udløser den farveskiftende kaskade af nye farvestoffer 1000 gange. Kredit:Tsuyoshi Kawai Et nyt reaktionssystem kan registrere røntgenstråler -
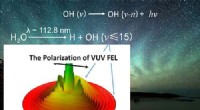 Undersøgelse afslører vandfotolyse og dets bidrag til hydroxyldagglødemissioner i atmosfæren på…Dalian kohærent lyskilde afslører vandfotolyse og dets bidrag til hydroxyldagglødemissioner i atmosfæren på Jorden og Mars. Kredit:CHANG Yao Jordens himmel viser en svag luminescens kendt som airg
Undersøgelse afslører vandfotolyse og dets bidrag til hydroxyldagglødemissioner i atmosfæren på…Dalian kohærent lyskilde afslører vandfotolyse og dets bidrag til hydroxyldagglødemissioner i atmosfæren på Jorden og Mars. Kredit:CHANG Yao Jordens himmel viser en svag luminescens kendt som airg -
 Ny undersøgelse afslører, at protonhydreringsstrukturer er asymmetriskeKredit:CC0 Public Domain Hvordan vand solvaterer og transporterer protoner er et grundlæggende spørgsmål, som både kemikere og biologer står over for, og det er afgørende for vores forståelse af p
Ny undersøgelse afslører, at protonhydreringsstrukturer er asymmetriskeKredit:CC0 Public Domain Hvordan vand solvaterer og transporterer protoner er et grundlæggende spørgsmål, som både kemikere og biologer står over for, og det er afgørende for vores forståelse af p


