Hvad er ikke -organiske forbindelser?
Ikke-organiske forbindelser:Den uorganiske verden
organiske forbindelser er dem, der indeholder kulstof, og typisk også brint. De er ofte komplekse og forskellige og danner livsgrundlaget, som vi kender det.
Ikke-organiske forbindelser på den anden side er forbindelser, der ikke indeholder carbon . De kan være enkle eller komplekse, og de findes i en lang række former.
Her er en sammenbrud af ikke-organiske forbindelser:
1. Nøgleegenskaber:
* Mangel på kulstof: Dette er det definerende kendetegn for ikke-organiske forbindelser.
* forskellige elementer: De kan omfatte en lang række elementer som ilt, nitrogen, brint, klor, natrium osv.
* bred vifte af ejendomme: Ikke-organiske forbindelser udviser en lang række egenskaber, fra faste stoffer til væsker til gasser, med forskellige farver, strukturer og reaktivitet.
2. Typer af ikke-organiske forbindelser:
* Oxider: Forbindelser indeholdende ilt og et andet element (f.eks. Vand (H₂O), kuldioxid (CO₂)).
* syrer: Forbindelser, der donerer hydrogenioner (H+) i opløsning (f.eks. Svovlsyre (H₂so₄), salpetersyre (HNO₃)).
* baser: Forbindelser, der accepterer hydrogenioner (H+) i opløsning (f.eks. Natriumhydroxid (NaOH), kaliumhydroxid (KOH)).
* salte: Forbindelser dannet ved reaktion af en syre og en base (f.eks. Natriumchlorid (NaCl), calciumcarbonat (Caco₃)).
* Metaller: Elementer, der generelt er skinnende, formbare og gode ledere af varme og elektricitet (f.eks. Jern (Fe), kobber (Cu), guld (AU)).
* ikke-metaler: Elementer, der mangler metalliske egenskaber (f.eks. Oxygen (O), svovl (er), klor (CL)).
3. Betydningen af ikke-organiske forbindelser:
* essentiel for livet: Mange ikke-organiske forbindelser spiller vigtige roller i biologiske processer (f.eks. Vand, salte, mineraler).
* Industrielle anvendelser: Ikke-organiske forbindelser er afgørende i forskellige industrier, fra konstruktion til medicin til fremstilling.
* Miljøpåvirkning: Ikke-organiske forbindelser kan have betydelige påvirkninger på miljøet, både positive og negative (f.eks. Forurening, gødning).
Eksempler på ikke-organiske forbindelser:
* Vand (H₂O)
* Kuldioxid (co₂)
* Natriumchlorid (NaCl)
* Jern (Fe)
* Ammoniak (NH₃)
* Silica (sio₂)
* Svovlsyre (H₂so₄)
Husk: Dette er en forenklet oversigt over ikke-organiske forbindelser. Kemiens verden er enorm og kompleks med mange undtagelser og nuancer.
Sidste artikelEr Francium en god varmeafdeling?
Næste artikelHvad er kogepunktets grader i Fahrenheit?
 Varme artikler
Varme artikler
-
 Forskere koder Wizard of Oz i en forsvindende lille plastikForskere gemte data i den kemiske struktur af en polymer, blandede dem i blækket i et personligt brev, sendte det med post og var i stand til at hente en kompleks krypteringsnøgle og dekryptere en kop
Forskere koder Wizard of Oz i en forsvindende lille plastikForskere gemte data i den kemiske struktur af en polymer, blandede dem i blækket i et personligt brev, sendte det med post og var i stand til at hente en kompleks krypteringsnøgle og dekryptere en kop -
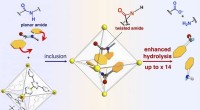 En molekylær trykkoger mører hårde stykker protein og hjælper med at bide afEt skema for reaktionshastighedsacceleration af amidhydrolyse ved inklusion i det selvsamlede molekylære bur. Kredit:NINS/IMS Proteiner består af aminosyrer forbundet med amidbindinger. Amidbindin
En molekylær trykkoger mører hårde stykker protein og hjælper med at bide afEt skema for reaktionshastighedsacceleration af amidhydrolyse ved inklusion i det selvsamlede molekylære bur. Kredit:NINS/IMS Proteiner består af aminosyrer forbundet med amidbindinger. Amidbindin -
 Hvad gør et kemikalie? Adressering af misforståelser om kemiKredit:Hans Renier/Unsplacsh, CC BY-SA Når jeg præsenterer mig selv som ph.d. studerende i kemi, Jeg kan ofte se frygt og uforståelighed i folks øjne:kemikere er ofte afbildet som skøre forskere,
Hvad gør et kemikalie? Adressering af misforståelser om kemiKredit:Hans Renier/Unsplacsh, CC BY-SA Når jeg præsenterer mig selv som ph.d. studerende i kemi, Jeg kan ofte se frygt og uforståelighed i folks øjne:kemikere er ofte afbildet som skøre forskere, -
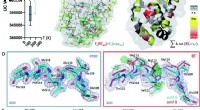 Sammenligning af kryogene strukturer med stuetemperaturprøver kan hjælpe med at identificere fejl …Fig. 1 Globale og lokale strukturelle reaktioner på temperatur. (A) Globalt, strukturer ved kryogene temperaturer (cryo; blå plot) er mere variable og mere kompakte end deres stuetemperatur (RT; røde
Sammenligning af kryogene strukturer med stuetemperaturprøver kan hjælpe med at identificere fejl …Fig. 1 Globale og lokale strukturelle reaktioner på temperatur. (A) Globalt, strukturer ved kryogene temperaturer (cryo; blå plot) er mere variable og mere kompakte end deres stuetemperatur (RT; røde
- Forskere udvikler fleksible, strækbare fotoniske enheder
- Er partikler af en gas tæt sammen?
- Hvordan transmitteres kemiske signaler over cellemembranen?
- Hvordan tappes energi fra vulkaner som elektricitetskilder?
- <p> Boxelder-bugs (Boisea trivittatis) samles i stort antal på siderne af huse og bygninger for at …
- Ultratynde selvhelbredende polymerer skaber nye, bæredygtige vandafvisende belægninger


