Ville du forvente, at klorpunktet for klor er højere eller lavere, end den jod forklarer?
* Intermolekylære kræfter: Styrken af intermolekylære kræfter (kræfterne mellem molekyler) spiller en afgørende rolle i bestemmelsen af kogepunktet. Stærkere intermolekylære kræfter kræver mere energi til at overvinde, hvilket fører til højere kogepunkter.
* London Dispersion Forces: Den primære intermolekylære kraft mellem klor (CL₂) og jod (I₂) molekyler er London -spredningskræfter. Disse kræfter stammer fra midlertidige udsving i elektronfordeling omkring molekylerne, hvilket skaber midlertidige dipoler, der inducerer dipoler i nabolande molekyler.
* størrelse og polariserbarhed: Jod er et meget større atom end klor. Større atomer har flere elektroner og en større elektronsky, hvilket gør dem mere polariserbare (lettere at inducere en midlertidig dipol). Dette betyder, at jodmolekyler oplever stærkere London -spredningskræfter sammenlignet med klormolekyler.
* kogepunkttrend: Når du bevæger dig ned ad halogengruppen (F, CL, BR, I), øges atomstørrelsen, og styrken i London -spredningskræfterne øges. Dette fører til en tendens til at øge kogepunkter, når du går ned i gruppen.
Kortfattet: Jod har stærkere London -spredningskræfter på grund af dens større størrelse og højere polariserbarhed, hvilket resulterer i et højere kogepunkt sammenlignet med klor.
 Varme artikler
Varme artikler
-
 Ny eksfolieringsteknik genvinder biomaterialers piezoelektricitetZhang Zhuomin, et medlem af Dr. Yang Zhengbaos forskerhold, demonstrerer råmaterialet i tyndtarmens submucosa fra får. Kredit:City University of Hong Kong Piezoelektriske materialer er anvendelige
Ny eksfolieringsteknik genvinder biomaterialers piezoelektricitetZhang Zhuomin, et medlem af Dr. Yang Zhengbaos forskerhold, demonstrerer råmaterialet i tyndtarmens submucosa fra får. Kredit:City University of Hong Kong Piezoelektriske materialer er anvendelige -
 Undersøgelse af elefant, capybara, menneskehår finder ud af, at tykkere hår ikke altid er stærke…Billedet viser, hvordan proteinfibre i menneskehårets cortex delaminerer, når håret går i stykker, tyder på brud på menneskehår i forskydningstilstand. Kredit:Wen Yang På trods af at være fire gan
Undersøgelse af elefant, capybara, menneskehår finder ud af, at tykkere hår ikke altid er stærke…Billedet viser, hvordan proteinfibre i menneskehårets cortex delaminerer, når håret går i stykker, tyder på brud på menneskehår i forskydningstilstand. Kredit:Wen Yang På trods af at være fire gan -
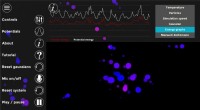 Smartphone-app bringer atomer og molekyler til live som aldrig førKredit:University of Sheffield En ny smartphone-app, der gør det muligt for folk at se, hvordan atomer og molekyler bevæger sig i verden omkring dem i hidtil uset detalje, er blevet udviklet af fo
Smartphone-app bringer atomer og molekyler til live som aldrig førKredit:University of Sheffield En ny smartphone-app, der gør det muligt for folk at se, hvordan atomer og molekyler bevæger sig i verden omkring dem i hidtil uset detalje, er blevet udviklet af fo -
 En ubrydelig kombination af usynlig blæk og kunstig intelligensMed almindelig blæk, en computer trænet med kodebogen afkoder STOP (øverst); når der vises et UV-lys på papiret, det usynlige blæk er blotlagt, og det rigtige budskab afsløres som BEGIN (nederst). Kre
En ubrydelig kombination af usynlig blæk og kunstig intelligensMed almindelig blæk, en computer trænet med kodebogen afkoder STOP (øverst); når der vises et UV-lys på papiret, det usynlige blæk er blotlagt, og det rigtige budskab afsløres som BEGIN (nederst). Kre
- Halvsyntetiske bakterier udskiller unaturlige proteiner
- Forskere rapporterer høj bærermobilitet af kubisk borarsenid
- Undersøgelse baner vejen for oprettelse af tænd- og slukknapper til kemiske reaktioner
- Sociale boliger viste sig at give de samme følelsesmæssige og praktiske fordele som boligejerskab
- Hvorfor kaldes cyklusser i biosfæren biogeokemiske cyklusser?
- Simuleringer viser, at en enkelt foton kan excitere to atomer samtidigt


