Hvad ellers er til fælles med calciumcarbonat og saltsyre?
1. Kemisk reaktion og produkter: De reagerer sammen for at danne calciumchlorid (CACL2), vand (H2O) og kuldioxid (CO2) gas. Denne reaktion er et klassisk eksempel på en dobbeltfortrængning reaktion, hvor ioner fra begge reaktanter skifter partnere.
2. Syre-base natur: Calciumcarbonat er en base , mens saltsyre er en syre . Dette er en grundlæggende forskel, men det er vigtigt, fordi det er drivkraften bag deres reaktion. Syren (HCI) donerer en proton (H+) til basen (CACO3), hvilket fører til dannelsen af de ovenfor nævnte produkter.
3. Ansøgninger: Begge forbindelser har forskellige applikationer inden for forskellige felter:
* calciumcarbonat: Meget brugt i konstruktion (cement, beton), landbrug (jordændring), farmaceutiske stoffer (antacida) og forskellige industrier (papir, maling, plast).
* Hydrochlorsyre: Afgørende i kemiske industrier (syntese, behandling), metalrensning og forskellige industrielle anvendelser.
4. Sikkerhedsmæssige bekymringer: Begge forbindelser kan udgøre sikkerhedsrisici, hvis de håndteres forkert:
* calciumcarbonat: Generelt betragtet som sikkert i små mængder, men kan forårsage åndedrætsirritation i store mængder.
* Hydrochlorsyre: Meget ætsende og kan forårsage alvorlige forbrændinger. Det er vigtigt at håndtere det med passende sikkerhedsforholdsregler.
5. Fysisk udseende:
* calciumcarbonat: Normalt findes som et hvidt pulver eller fast stof, men det kan også eksistere i forskellige former som kalsit, aragonit og kridt.
* Hydrochlorsyre: En farveløs væske med en skarp lugt.
Mens både calciumcarbonat og saltsyre har karakteristiske egenskaber og anvendelser, resulterer deres interaktion i en velkendt og vigtig kemisk reaktion, der har konsekvenser på tværs af forskellige felter.
Sidste artikelHvad er molekylær formel for sølvnitrat?
Næste artikelHvad er de 8 mest almindelige gasser i atmosfæren?
 Varme artikler
Varme artikler
-
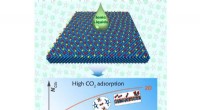 Todimensionelle ioniske væsker til effektivt at opfange kuldioxidDen ultrahøje CO2 adsorptionskapacitet af todimensionelle ioniske væsker. Kredit:IPE I forbindelse med globale bekymringer om klimaændringer og drivhusgaskontrol, en ny teknologi til CO2 fangst, ud
Todimensionelle ioniske væsker til effektivt at opfange kuldioxidDen ultrahøje CO2 adsorptionskapacitet af todimensionelle ioniske væsker. Kredit:IPE I forbindelse med globale bekymringer om klimaændringer og drivhusgaskontrol, en ny teknologi til CO2 fangst, ud -
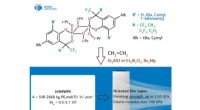 En undersøgelse af katalysatorer til syntetisering af polyethylen med ultrahøj molekylvægtKredit:RUDN Universitet En kemiker fra RUDN University som en del af et team af forskere har syntetiseret nye højaktive katalysatorer til fremstilling af polyethylen med ultrahøj molekylvægt, som
En undersøgelse af katalysatorer til syntetisering af polyethylen med ultrahøj molekylvægtKredit:RUDN Universitet En kemiker fra RUDN University som en del af et team af forskere har syntetiseret nye højaktive katalysatorer til fremstilling af polyethylen med ultrahøj molekylvægt, som -
 Ingeniører designer kunstig synapse til hjerne-på-en-chip-hardwareFra venstre:MIT-forskere Scott H. Tan, Jeehwan Kim, og Shinhyun Choi Kredit:Kuan Qiao Når det kommer til processorkraft, den menneskelige hjerne kan bare ikke slås. Pakket i squishy, organer på s
Ingeniører designer kunstig synapse til hjerne-på-en-chip-hardwareFra venstre:MIT-forskere Scott H. Tan, Jeehwan Kim, og Shinhyun Choi Kredit:Kuan Qiao Når det kommer til processorkraft, den menneskelige hjerne kan bare ikke slås. Pakket i squishy, organer på s -
 Knækker den katalytiske kodeKredit:Argonne National Laboratory Den nyudviklede evne til at udnytte tidligere utilgængelige skifergasforekomster i løbet af det sidste årti har skabt en rigelig kilde af gasser, herunder metan,
Knækker den katalytiske kodeKredit:Argonne National Laboratory Den nyudviklede evne til at udnytte tidligere utilgængelige skifergasforekomster i løbet af det sidste årti har skabt en rigelig kilde af gasser, herunder metan,
- Billede:Hubble finder en Einstein -ring
- Antibiotika kan reducere immuncellernes evne til at dræbe bakterier
- Forskere knækker mysteriet om hvirvlende hvirvler i ægceller
- Hvilken væske ruster en krone hurtigere eddike eller saltvand?
- Hvilken af disse arter har en længere binding B2 eller B2?
- Kan jeg tage et lægemiddel for at udslette en bestemt hukommelse?


