Hvorfor kan ikke calciumcarbonat CACO4 udføre elektriskitet, når den blandes med deioniseret vand?
1. Calciumcarbonats struktur:
* Calciumcarbonat er en ionisk forbindelse . Dette betyder, at det dannes af den elektrostatiske tiltrækning mellem positivt ladede calciumioner (Ca²⁺) og negativt ladede carbonationer (co₃²⁻).
* Disse ioner holdes sammen i en stiv, krystallinsk struktur. Denne struktur tillader ikke fri bevægelighed for afgifter, hvilket er nødvendigt for elektrisk ledningsevne.
2. Deioniserede vandets rolle:
* Deioniseret vand er i det væsentlige rent vand med minimale opløste ioner. Det er en dårlig leder af elektricitet, fordi der er meget få ladede partikler til at bære strømmen.
* Mens calciumcarbonat er lidt opløseligt i vand, er det beløb, der opløses, ekstremt lille. Dette betyder, at der ikke er nok fri calcium- og carbonationer i opløsning til markant at forbedre ledningsevnen af det deioniserede vand.
3. Hvorfor nogle forbindelser udfører elektricitet:
* Nogle forbindelser, som salte, udfører elektricitet, når de opløses i vand, fordi deres ioner adskiller sig (separate) i opløsning. Dette skaber en pulje af gratis, mobile ladninger, der kan bære en elektrisk strøm.
* For eksempel opløses natriumchlorid (NaCl) i vand til dannelse af Na⁺ og Cl⁻ioner. Disse ioner kan bevæge sig frit, hvilket gør det muligt for løsningen at udføre elektricitet.
I resuméet udfører calciumcarbonat, selv når det blandes med deioniseret vand, ikke elektricitet, fordi dets ioniske struktur og lav opløselighed forhindrer dannelse af nok frie ioner til at bære en elektrisk strøm.
 Varme artikler
Varme artikler
-
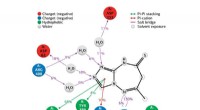 Chemist syntetiserer nye forbindelser med stærke antidiabetiske egenskaberKredit:RUDN Universitet En kemiker fra RUDN University har syntetiseret nye derivater af 1, 2, 4-triazol, der udviser antidiabetiske egenskaber. Eksperimenter viste, at disse forbindelser virker b
Chemist syntetiserer nye forbindelser med stærke antidiabetiske egenskaberKredit:RUDN Universitet En kemiker fra RUDN University har syntetiseret nye derivater af 1, 2, 4-triazol, der udviser antidiabetiske egenskaber. Eksperimenter viste, at disse forbindelser virker b -
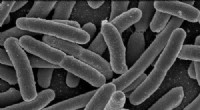 Det klareste billede nogensinde af cellemembranen giver uventet struktur, forskningsmulighederEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH Arbejde med en nobelprisvindende biofysiker, et team af forskere ved Virginia Commonwealth University har fået den klareste opfatte
Det klareste billede nogensinde af cellemembranen giver uventet struktur, forskningsmulighederEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH Arbejde med en nobelprisvindende biofysiker, et team af forskere ved Virginia Commonwealth University har fået den klareste opfatte -
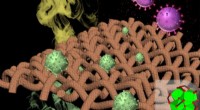 En sjælden bedrift:Materiale beskytter mod både biologiske og kemiske truslerProgrammerbar krystallinsk svamp-tekstil komposit til eliminering af biologiske og kemiske trusler. Kredit:Northwestern University Et forskningshold fra Northwestern University har udviklet et als
En sjælden bedrift:Materiale beskytter mod både biologiske og kemiske truslerProgrammerbar krystallinsk svamp-tekstil komposit til eliminering af biologiske og kemiske trusler. Kredit:Northwestern University Et forskningshold fra Northwestern University har udviklet et als -
 Opfindelsen af bittesmå organiske film kunne muliggøre ny elektronikForskere opdagede en ny metode til at samle tusindvis af organiske molekyler til en glat flad film, kun få nanometer tyk, vist her i denne illustration. Kredit:Baorui Cheng Den første mobiltelefon
Opfindelsen af bittesmå organiske film kunne muliggøre ny elektronikForskere opdagede en ny metode til at samle tusindvis af organiske molekyler til en glat flad film, kun få nanometer tyk, vist her i denne illustration. Kredit:Baorui Cheng Den første mobiltelefon
- Hvad er en stille vulkan?
- Kickstartende Moores lov? Ny syntetisk metode til fremstilling af mikrochips kunne hjælpe
- Nogle revøer, der er modstandsdygtige over for klimaændringer:undersøgelse
- Retten blokerer for, at Ryanair-piloter strejker i Irland
- Hvilke slags intermolekylære kræfter er til stede i en blanding af lithiumphosphat og methanol (CH…
- Hvordan er Reptiler & Amfibier ens?


