Hvad er det teoretiske udbytte af aluminium, der kan produceres ved reaktion 60,0 g oxid med 30,0 carbon i henhold til følgende kemiske Al2O3 3C 2al 3CO?
1. Afbalanceret kemisk ligning:
Den afbalancerede kemiske ligning er allerede tilvejebragt:
Al₂o₃ + 3c → 2al + 3co
2. Beregn mol af reaktanter:
* mol Al₂o₃:
- Molmasse Al₂o₃ =(2 * 26,98 g/mol) + (3 * 16,00 g/mol) =101,96 g/mol
- mol Al₂o₃ =(60,0 g) / (101,96 g / mol) =0,588 mol
* mol C:
- Molmasse på C =12,01 g/mol
- mol C =(30,0 g) / (12,01 g / mol) =2,498 mol
3. Bestem den begrænsende reaktant:
* Sammenlign molforholdene: Den afbalancerede ligning viser, at 1 mol al₂o₃ reagerer med 3 mol C.
* Beregn de krævede mol på C: 0,588 mol al₂o₃ * (3 mol C / 1 mol al₂o₃) =1,764 mol C
* Konklusion: Vi har flere mol C (2,498 mol) end nødvendigt (1,764 mol) til reaktionen. Derfor er Al₂o₃ den begrænsende reaktant.
4. Beregn teoretisk udbytte af aluminium:
* molforhold: Fra den afbalancerede ligning producerer 1 mol Al₂o₃ 2 mol Al.
* mol Al: 0,588 mol al₂o₃ * (2 mol al / 1 mol al₂o₃) =1,176 mol al
* masse af Al: 1.176 mol al * (26,98 g/mol) = 31,7 g al
Derfor er det teoretiske udbytte af aluminium, der kan produceres, 31,7 g.
 Varme artikler
Varme artikler
-
 Undersøgelse af nitrogen-doterede polycykliske aromatiske kulbrinter til højtydende OLED'erInden for de nye OLEDer lyser forskerne selv det mørkeste mørke op. Billedet er taget af Neonmuseet i Warszawa. Kredit:Kilde IPC PAS, Grzegorz Krzyzewski Elektroniske visuelle skærme er kommet lang
Undersøgelse af nitrogen-doterede polycykliske aromatiske kulbrinter til højtydende OLED'erInden for de nye OLEDer lyser forskerne selv det mørkeste mørke op. Billedet er taget af Neonmuseet i Warszawa. Kredit:Kilde IPC PAS, Grzegorz Krzyzewski Elektroniske visuelle skærme er kommet lang -
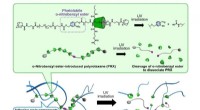 Vendbar klæbrighed i tandcement er noget at smile afKredit:Institut for Organiske Biomaterialer, TMDU Alle, der har fået fyldt tandhuller, ved, at de bedste tandmaterialer bliver, hvor tandlægen lægger dem. Vedhæftningen af i øjeblikket tilgængel
Vendbar klæbrighed i tandcement er noget at smile afKredit:Institut for Organiske Biomaterialer, TMDU Alle, der har fået fyldt tandhuller, ved, at de bedste tandmaterialer bliver, hvor tandlægen lægger dem. Vedhæftningen af i øjeblikket tilgængel -
 Kemisk innovation stabiliserer den bedst ydende perovskit-formuleringUdgiver i Videnskab , forskere ved EPFL har med succes overvundet et begrænsende problem med at stabilisere den bedst ydende formulering af metalhalogenid perovskitfilm, en nøglespiller i en række a
Kemisk innovation stabiliserer den bedst ydende perovskit-formuleringUdgiver i Videnskab , forskere ved EPFL har med succes overvundet et begrænsende problem med at stabilisere den bedst ydende formulering af metalhalogenid perovskitfilm, en nøglespiller i en række a -
 Udvidelse af biosyntesevejen via retrobiosynteseBiosyntetiske reaktioner konstrueret i E. coli til in vivo produktion af 12 SCPAer. Disse 12 SCPAer var dem, der viste sig at blive produceret af valin decarboxylase (VlmD) in vitro (stiplede kasser).
Udvidelse af biosyntesevejen via retrobiosynteseBiosyntetiske reaktioner konstrueret i E. coli til in vivo produktion af 12 SCPAer. Disse 12 SCPAer var dem, der viste sig at blive produceret af valin decarboxylase (VlmD) in vitro (stiplede kasser).
- Hvor farlig er ekstrem varme for mennesker?
- Hvilken er mesterkirtel hos mennesker?
- Højtermoresistente biopolyimider bliver vandopløselige som stivelse
- Hvordan påvirker skyafdækningen vejret på overfladen?
- Hurtige gasudbrud opdaget i hvid dværgstjerne for første gang
- Hvad sagde Niel Armstrong, da han landede på månen?


