Hvorfor er ammoniumchloridopløselig i vand?
1. Ion-dipol-interaktioner:
* Ammoniumchlorid er en ionisk forbindelse, hvilket betyder, at det findes som ioner (NH₄⁺ og CL⁻) i sin faste form.
* Vand er et polært molekyle med en delvis positiv ladning på brintatomerne og en delvis negativ ladning på iltatomet.
* De positivt ladede ammoniumioner (NH₄⁺) tiltrækkes af det negativt ladede iltatom af vandmolekyler.
* Tilsvarende tiltrækkes de negativt ladede chloridioner (CL⁻) af de positivt ladede hydrogenatomer af vandmolekyler.
* Disse stærke ion-dipol-interaktioner overvinder de ioniske kræfter, der holder ammoniumchloridkrystallen sammen, så den kan opløses.
2. Hydrering:
* Når ammoniumchlorid opløses i vand, omgiver vandmolekyler ionerne og danner en hydratiseringsskal.
* Denne hydratiseringsproces svækker de ioniske bindinger i ammoniumchloridkrystallen og hjælper med at holde ionerne adskilt i opløsning.
3. Entropi:
* Opløsningen af ammoniumchlorid i vand øger systemets entropi (lidelse).
* Denne stigning i entropi er gunstig og bidrager til opløseligheden af saltet.
generelt:
Kombinationen af stærke ion-dipol-interaktioner, hydrering af ioner og entropiforøgelsen forbundet med opløsning af ammoniumchlorid i vand fører til dets høje opløselighed.
 Varme artikler
Varme artikler
-
 Hvad er peberspray?Kredit:The American Chemical Society Uanset om det er at gå ned ad en mørk gade om natten eller kæmpe mod grizzlybjørne på stien, peberspray er et effektivt redskab til at afværge en angriber og k
Hvad er peberspray?Kredit:The American Chemical Society Uanset om det er at gå ned ad en mørk gade om natten eller kæmpe mod grizzlybjørne på stien, peberspray er et effektivt redskab til at afværge en angriber og k -
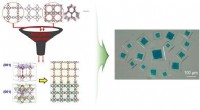 Algoritme identificerer optimale par til at sammensætte metal-organiske rammerFigur:Et eksempel på en rationelt syntetiseret MOF@MOFs (kubisk HKUST-1@MOF-5 ). Kredit:Korea Advanced Institute of Science and Technology (KAIST) Integrationen af metal-organiske rammer (MOFer
Algoritme identificerer optimale par til at sammensætte metal-organiske rammerFigur:Et eksempel på en rationelt syntetiseret MOF@MOFs (kubisk HKUST-1@MOF-5 ). Kredit:Korea Advanced Institute of Science and Technology (KAIST) Integrationen af metal-organiske rammer (MOFer -
 Modellering af evigheden i stenlaboratorietUdforskningstunnel i Mont Terri internationale stenlaboratorium. Siden 1996, klippeformationer, der kunne spille en rolle i opbevaring af radioaktivt affald, er blevet undersøgt her. Kredit:BGR Nå
Modellering af evigheden i stenlaboratorietUdforskningstunnel i Mont Terri internationale stenlaboratorium. Siden 1996, klippeformationer, der kunne spille en rolle i opbevaring af radioaktivt affald, er blevet undersøgt her. Kredit:BGR Nå -
 Måling af eliminering af plastikpartikler fra kroppen hos musFigur 1. PET-CT billeder af mus ved 6, 12, 24, og 48 timer efter oral administration af 20 nm polystyrenpartikler (øverste række) og 1 µm polystyrenpartikler (nederste række). Grøn kant:MIP, blå kant:
Måling af eliminering af plastikpartikler fra kroppen hos musFigur 1. PET-CT billeder af mus ved 6, 12, 24, og 48 timer efter oral administration af 20 nm polystyrenpartikler (øverste række) og 1 µm polystyrenpartikler (nederste række). Grøn kant:MIP, blå kant:
- Planetforskere opdager beviser for en reduceret atmosfære på oldtidens Mars
- Hvordan man laver en model til et øret for børn
- Energiafledning fra vibrerende guldnanopartikler stærkt påvirket af det omgivende miljø
- Hvordan er encellede organismer bedre end flercellede organismer?
- Hvor meget jern er der ca. på jorden?
- Hvordan måles afstande i rummet?


