Har kloratom en mindre radius end ion?
* atomradius: Atomradiusen henviser til afstanden fra kernen til den yderste elektronskal af et atom.
* ionisk radius: Den ioniske radius henviser til afstanden fra kernen til den yderste elektronskal af en ion.
kloratom: Et kloratom har 17 elektroner og 17 protoner. Den yderste skal har 7 elektroner.
chloridion (cl⁻): Når et chloratom får et elektron til dannelse af en chloridion, har det nu 18 elektroner og 17 protoner. Denne ekstra elektron går ind i den yderste skal, hvilket gør den mere negativt ladet og forårsager en større frastødning mellem elektronerne. Denne frastødning skubber elektronskaller længere væk fra kernen, hvilket resulterer i en større ionisk radius sammenlignet med atomradius.
Kortfattet:
* cl atom: Mindre radius (på grund af færre elektroner og mindre frastødelse)
* cl⁻ion: Større radius (på grund af flere elektroner og større frastødelse)
 Varme artikler
Varme artikler
-
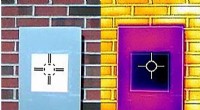 Den hvideste maling er her - og den er den sejeste. Bogstaveligt talt.Et infrarødt kamera viser, hvordan en prøve af den hvideste hvide maling (den mørke lilla firkant i midten) faktisk afkøler brættet under omgivelsestemperatur, noget, som ikke engang kommercielle varm
Den hvideste maling er her - og den er den sejeste. Bogstaveligt talt.Et infrarødt kamera viser, hvordan en prøve af den hvideste hvide maling (den mørke lilla firkant i midten) faktisk afkøler brættet under omgivelsestemperatur, noget, som ikke engang kommercielle varm -
 Forskere udvikler værktøj til hurtig diagnosticering af bakterielle infektionerMohammad Zarifi, en assisterende professor ved UBC Okanagan, viser sin lille biosensor, der kan bruges til at stille en realtidsdiagnose af en bakteriel infektion. Kredit:UBC Okanagan Ved hjælp af
Forskere udvikler værktøj til hurtig diagnosticering af bakterielle infektionerMohammad Zarifi, en assisterende professor ved UBC Okanagan, viser sin lille biosensor, der kan bruges til at stille en realtidsdiagnose af en bakteriel infektion. Kredit:UBC Okanagan Ved hjælp af -
 Forskere finder stor lineær negativ termisk ekspansion i intermetalliske Cr-Se-Te-forbindelserTemperaturafhængighed af volumenændringer af Cr-Te-Se med forskellige sammensætninger. Kredit:ZHENG Xinqi Forskere brugte et røntgendiffraktometer (XRD) med variabel temperatur på Kinas Steady Hig
Forskere finder stor lineær negativ termisk ekspansion i intermetalliske Cr-Se-Te-forbindelserTemperaturafhængighed af volumenændringer af Cr-Te-Se med forskellige sammensætninger. Kredit:ZHENG Xinqi Forskere brugte et røntgendiffraktometer (XRD) med variabel temperatur på Kinas Steady Hig -
 Video:Hvorfor har vi ikke syntetisk blod endnu?Kredit:The American Chemical Society Der doneres millioner af liter blod rundt om i verden hvert år, men der er stadig ikke nok til alle, der har brug for det. Kemikere har i et århundrede forsøgt
Video:Hvorfor har vi ikke syntetisk blod endnu?Kredit:The American Chemical Society Der doneres millioner af liter blod rundt om i verden hvert år, men der er stadig ikke nok til alle, der har brug for det. Kemikere har i et århundrede forsøgt
- En stående bølge dannes i en strakt snor, der er 2,3 meter lang. Hvad er bølgelængden af førs…
- En ny vej til at forstå anden lyd i Bose-Einstein-kondensater
- Når der dannes to toner af frekvenser F1 og F2 afre lyd sammen dyr sammen, hvis hvad vil være frek…
- Observation, simulering, og AI går sammen for at afsløre et klart univers
- Thunder and Lightning Activities for Kids
- Ny forskning hjælper med at forklare, hvorfor piger klarer sig bedre i skolen


