Hvilket element reagerer med H2O for at producere H2?
Her er hvorfor:
* alkalimetaller er meget reaktive metaller placeret i gruppe 1 i den periodiske tabel (lithium, natrium, kalium, rubidium, cæsium og francium).
* De har en stærk tendens til at miste deres enkelt valenselektron, hvilket gør dem til fremragende reduktionsmidler.
* Når alkalimetaller reagerer med vand, fortrænger de brint fra vandmolekyler, danner brintgas og et metalhydroxid.
Her er en generel ligning for reaktionen:
2m + 2h₂o → 2moh + H₂
Hvor:
* M repræsenterer et alkalimetal.
* MOH repræsenterer metalhydroxid.
Eksempel:
* natrium (NA) reagerer med vand:
2na + 2h₂o → 2naoh + h₂
Denne reaktion er meget eksoterm, hvilket betyder, at den frigiver en masse varme, hvilket endda kan få brintgassen til at antænde.
Bemærk: Andre metaller som calcium, magnesium og zink reagerer også med vand for at producere brintgas, men de kræver specifikke tilstande, såsom opvarmning eller damp.
Sidste artikelHvilket element ville være mere reaktivt end magnesium?
Næste artikelHvad er den sidste af alkaliske jordmetaller?
 Varme artikler
Varme artikler
-
 Enkel metode til at omdanne kuldioxid til nyttige forbindelserMed den nye metode kuldioxid omdannes til nyttige porøse komplekser (PCPer/MOFer) ved stuetemperatur og uden højt tryk. Kredit:Mindy Takamiya/Kyoto University iCeMS Forskere i Japan har fundet en
Enkel metode til at omdanne kuldioxid til nyttige forbindelserMed den nye metode kuldioxid omdannes til nyttige porøse komplekser (PCPer/MOFer) ved stuetemperatur og uden højt tryk. Kredit:Mindy Takamiya/Kyoto University iCeMS Forskere i Japan har fundet en -
 Fuld af varm luft og stolt over det:Forbedring af gaslagring med MOF'erIdealiseret interpenetreret MOF -struktur. Den sammenfiltrede MOF kan sprede varme omtrent to gange hurtigere, end de bestanddele MOF kan separat, muligvis muliggør mere effektiv gaslagring. Kredit:Sw
Fuld af varm luft og stolt over det:Forbedring af gaslagring med MOF'erIdealiseret interpenetreret MOF -struktur. Den sammenfiltrede MOF kan sprede varme omtrent to gange hurtigere, end de bestanddele MOF kan separat, muligvis muliggør mere effektiv gaslagring. Kredit:Sw -
 Laboratoriegennembrud inden for 3-D print af glasEn ny 3D-printteknik, udviklet hos Lawrence Livermore, kunne tillade videnskabsmænd at udskrive glas, der inkorporerer forskellige brydningsindekser i en enkelt flad optik, gør efterbehandling billige
Laboratoriegennembrud inden for 3-D print af glasEn ny 3D-printteknik, udviklet hos Lawrence Livermore, kunne tillade videnskabsmænd at udskrive glas, der inkorporerer forskellige brydningsindekser i en enkelt flad optik, gør efterbehandling billige -
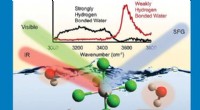 Unik grænseflade og uventet adfærd hjælper med at forklare, hvordan tungmetaller virkerForskere identificerede tre forskellige typer vandmolekyler, der omgiver en tung, anionisk metalchloridkompleks (nederst) ved brug af spektroskopi (øverst) ved en luft/vand-grænseflade. Hver type vand
Unik grænseflade og uventet adfærd hjælper med at forklare, hvordan tungmetaller virkerForskere identificerede tre forskellige typer vandmolekyler, der omgiver en tung, anionisk metalchloridkompleks (nederst) ved brug af spektroskopi (øverst) ved en luft/vand-grænseflade. Hver type vand
- Hvorfor siger vi, at jorden er livets fundament?
- Hvis et papirklip gnides i en retning mod stærk magnet, hvad er årsagen til at forekomme klip?
- Hvad er et substantiv for videnskabelig?
- Virgin Australia til at gå i administration:kilde
- Denne hydrogeltablet kan rense en liter flodvand på en time
- Slavehandelens indvirkning på den hollandske økonomi


