Hvad er chloridionen og chloratomelektronkonfigurationen?
kloratom (CL)
* atomnummer: 17, hvilket betyder, at det har 17 protoner og 17 elektroner.
* Elektronkonfiguration: 1S² 2S² 2P⁶ 3S² 3P⁵
Forklaring:
* Elektronkonfigurationen følger Aufbau -princippet og Hunds regel og udfylder orbitaler i rækkefølge af stigende energi.
* 1S²: Det første energiniveau (n =1) har to elektroner i 1'erne orbital.
* 2s²: Det andet energiniveau (n =2) har to elektroner i 2'erne orbital.
* 2p⁶: Det andet energiniveau har også seks elektroner i de tre 2p orbitaler.
* 3S²: Det tredje energiniveau (n =3) har to elektroner i 3'erne orbital.
* 3p⁵: Det tredje energiniveau har fem elektroner i de tre 3p orbitaler.
chloridion (cl⁻)
* dannelse: Klor vinder en elektron for at opnå en stabil oktet (otte elektroner) i sin ydre skal.
* Elektronkonfiguration: 1S² 2S² 2P⁶ 3S² 3P⁶
Forklaring:
* Chloridionen har nu 18 elektroner (17 originale + 1 opnået).
* Den tilsatte elektron fylder den sidste 3p orbital, hvilket giver den en fuld ydre skal.
Key Takeaway:
* Chloridionen er mere stabil end chloratomet, fordi det har en fuld ydre skal af elektroner.
 Varme artikler
Varme artikler
-
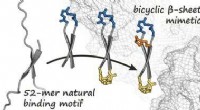 Cykliske protein-mimetika hæmmer onkogenet β-cateninKredit:Wiley Hæmningen af patologiske protein-protein-interaktioner er en lovende tilgang til behandling af et stort antal sygdomme, herunder mange former for kræft. Et team af forskere har nu u
Cykliske protein-mimetika hæmmer onkogenet β-cateninKredit:Wiley Hæmningen af patologiske protein-protein-interaktioner er en lovende tilgang til behandling af et stort antal sygdomme, herunder mange former for kræft. Et team af forskere har nu u -
 Svampemotorveje på osteskaller påvirker fødevaresikkerheden, modenhedSlim vokser på skallen af hulmodnet ost i Frankrig. Kredit:Benjamin Wolfe Bakterier, der bevæger sig langs svampemotorveje på osteskaller, kan spredes hurtigere og ødelægge kvaliteten eller forå
Svampemotorveje på osteskaller påvirker fødevaresikkerheden, modenhedSlim vokser på skallen af hulmodnet ost i Frankrig. Kredit:Benjamin Wolfe Bakterier, der bevæger sig langs svampemotorveje på osteskaller, kan spredes hurtigere og ødelægge kvaliteten eller forå -
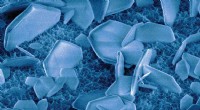 Vand spiller en uventet rolle i dannelsen af mineralerZinkoxidnanopartikler suspenderet i vand klikker sammen, når de er korrekt justeret og danner større krystaller (vist her). Kræfterne mellem partiklerne langs en specifik fastgørelsesretning blev målt
Vand spiller en uventet rolle i dannelsen af mineralerZinkoxidnanopartikler suspenderet i vand klikker sammen, når de er korrekt justeret og danner større krystaller (vist her). Kræfterne mellem partiklerne langs en specifik fastgørelsesretning blev målt -
 AlScN – alternativt materiale til mere effektiv smartphone-hardwareBearbejdede overflade akustiske bølgestrukturer (SAW) på AlScN/Si-lag (venstre) og AlScN/Al2O3-lag (højre). Kredit:Fraunhofer-Gesellschaft 5G mobile dataoverførsler kræver brug af flere og højere
AlScN – alternativt materiale til mere effektiv smartphone-hardwareBearbejdede overflade akustiske bølgestrukturer (SAW) på AlScN/Si-lag (venstre) og AlScN/Al2O3-lag (højre). Kredit:Fraunhofer-Gesellschaft 5G mobile dataoverførsler kræver brug af flere og højere
- Hvad fortæller antallet af protoner i et atom også?
- Stjernevals med dramatisk afslutning
- Natrium, ikke varme, afslører vulkansk aktivitet på Jupiters måne Io
- Sådan konverteres mol til Pressure
- Forskere ser frigivelse af kræftlægemidler fra DNA-nanostrukturer i realtid
- Robotmyrer bygger huse på Mars?


