Hvorfor er PH-skalaen 1-14 og ikke 1-10 eller noget mere intuitivt?
* logaritmisk skala: PH -skalaen er en logaritmisk skala, hvilket betyder, at hvert hele antal ændringer repræsenterer en ti gange ændring i koncentrationen af H+ -ioner. Dette giver os mulighed for at udtrykke en lang række surhedsgrad og alkalinitet på en håndterbar måde.
* Vands autoionisering: Vandet i sig selv kan ionisere lidt og producere H+ og ohioner. Produktet af deres koncentrationer er en konstant (KW) ved en given temperatur. Ved 25 ° C, kW =1 x 10^-14.
* neutral pH: Den neutrale pH på 7 svarer til lige koncentrationer af H+ og OH-ioner i vand. Dette skyldes, at kvadratroden på 1 x 10^-14 er 1 x 10^-7, hvilket repræsenterer koncentrationen af hver ion.
* ekstremer:
* ph 1: Repræsenterer en meget sur opløsning med en H+ -koncentration på 1 x 10^-1 M.
* ph 14: Repræsenterer en meget grundlæggende løsning med en H+ -koncentration på 1 x 10^-14 M.
Hvorfor ikke 1-10?
Brug af en 1-10 skala ville komprimere række af surhedsgrad og alkalinitet. Forskellen mellem en pH på 1 og 2 ville være meget større end forskellen mellem en pH på 9 og 10. Dette ville ikke nøjagtigt afspejle de faktiske ændringer i H+ -koncentration.
Kortfattet:
PH-skalaen er 1-14, fordi det er en logaritmisk skala baseret på koncentrationen af H+ -ioner i vand. Dette interval giver os mulighed for at udtrykke en lang række surhedsgrad og alkalinitet, mens vi opretholder et konsistent forhold mellem pH -værdier og H+ -koncentrationer.
Sidste artikelHvordan dannes nitrogenoxid af brændende benzin?
Næste artikelHvad er symbolet for nitrogenoxider?
 Varme artikler
Varme artikler
-
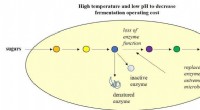 Forskere konstruerer hårdere mikrober for at forbedre bioproduktion af brændstoffer, kemikalierForskere arbejder på at identificere og producere robuste enzymer, der kan erstatte andre enzymer, der nedbrydes i gæringen af biobaserede brændstoffer og kemikalier. Kredit:Laura Jarboe. Travl,
Forskere konstruerer hårdere mikrober for at forbedre bioproduktion af brændstoffer, kemikalierForskere arbejder på at identificere og producere robuste enzymer, der kan erstatte andre enzymer, der nedbrydes i gæringen af biobaserede brændstoffer og kemikalier. Kredit:Laura Jarboe. Travl, -
 Mikrobølger afslører detaljeret struktur af molekylær motorSom en makroskopisk motor, det kunstige motormolekyle har en stator (nederst) og en rotor (øverst), forbundet med en aksel. Kredit:Sérgio Domingos / DESY Et team af forskere har brugt mikrobølger
Mikrobølger afslører detaljeret struktur af molekylær motorSom en makroskopisk motor, det kunstige motormolekyle har en stator (nederst) og en rotor (øverst), forbundet med en aksel. Kredit:Sérgio Domingos / DESY Et team af forskere har brugt mikrobølger -
 Ny bioinspireret lim binder enhver overflade under vandetKredit:Wageningen University &Research Undervandsadhæsion er teknisk udfordrende på grund af tilstedeværelsen af vand, den værste fjende for enhver lim. Nu, forskere fra Wageningen University &R
Ny bioinspireret lim binder enhver overflade under vandetKredit:Wageningen University &Research Undervandsadhæsion er teknisk udfordrende på grund af tilstedeværelsen af vand, den værste fjende for enhver lim. Nu, forskere fra Wageningen University &R -
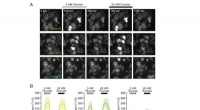 Grønne fluorescerende proteinbaserede glukoseindikatorer til overvågning af glukosemetabolisme i r…A:Billeder af HeLa -celler, der udtrykker Green Glifon50, Grøn Glifon600 og Grøn Glifon4000. Skalaen repræsenterer 20 μm. B:Ændringer i fluorescensintensitet (FI) i HeLa -celler, der udtrykker de tre
Grønne fluorescerende proteinbaserede glukoseindikatorer til overvågning af glukosemetabolisme i r…A:Billeder af HeLa -celler, der udtrykker Green Glifon50, Grøn Glifon600 og Grøn Glifon4000. Skalaen repræsenterer 20 μm. B:Ændringer i fluorescensintensitet (FI) i HeLa -celler, der udtrykker de tre
- Hvad bliver røde kæmper til, når de løber tør for brændstof?
- Massive isformationer, der begynder i høje højder og består af mange års snefald, smelter aldrig…
- Hvad er øen, der ligger halvdelen i Asien og Oceanien?
- Kviksølvundersøgelser afslører et spændende mål for BepiColombo
- Hvad brækker man en dobbelt helix af DNA?
- Hvordan en virus danner sine symmetriske skaller


