Er diamant en leder eller isolator?
Her er hvorfor:
* binding: Diamond har en meget stærk kovalent bindingsstruktur. Hvert carbonatom er tæt bundet til fire andre carbonatomer, der danner et stift gitter.
* Elektronmobilitet: Elektronerne i de kovalente bindinger holdes tæt og kan ikke bevæge sig frit. Dette betyder, at de ikke let kan bære en elektrisk strøm.
* båndgap: Diamond har et meget stort båndgap, hvilket betyder, at der kræves en masse energi for at begejstre et elektron til et ledningsbånd og give det mulighed for at bære en strøm.
Der er dog nogle undtagelser:
* Højtryksdiamant: Under ekstremt højt tryk kan Diamond blive en leder. Dette skyldes, at trykket kan ændre materialets elektroniske struktur.
* dopet diamant: Urenheder (som bor eller fosfor) kan føjes til Diamond for at gøre det semi-ledende. Denne proces kaldes doping.
Generelt betragtes Diamond som en meget god isolator i sin naturlige form.
 Varme artikler
Varme artikler
-
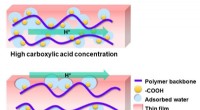 Protoners rejsevej i polymerer kan føre til rene brændstofferSkematisk repræsentation af afhængigheden af hovedprotontransportvejen i tynde polymerfilm af carboxylsyregruppekoncentrationen. Kredit:Yuki Nagao Protoner - subatomære partikler med en positiv
Protoners rejsevej i polymerer kan føre til rene brændstofferSkematisk repræsentation af afhængigheden af hovedprotontransportvejen i tynde polymerfilm af carboxylsyregruppekoncentrationen. Kredit:Yuki Nagao Protoner - subatomære partikler med en positiv -
 Forskere fremstiller gennemsigtig keramik af høj kvalitetKredit:CC0 Public Domain Mid-infrarøde lasere er blevet meget brugt til billeddannelse, opdagelse, diagnostik, miljøovervågning, medicin, industri, forsvar og andre. Til mellem-infrarøde lasersyst
Forskere fremstiller gennemsigtig keramik af høj kvalitetKredit:CC0 Public Domain Mid-infrarøde lasere er blevet meget brugt til billeddannelse, opdagelse, diagnostik, miljøovervågning, medicin, industri, forsvar og andre. Til mellem-infrarøde lasersyst -
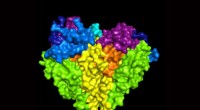 Team opdager molekylær kanal, der regulerer blodtrykketVed hjælp af et kryo-elektronmikroskop, forskere ved OHSU i Portland, Oregon, genereret en tredimensionel model af den humane epitheliale natriumkanal. Kanalen er kritisk til at kontrollere blodtrykke
Team opdager molekylær kanal, der regulerer blodtrykketVed hjælp af et kryo-elektronmikroskop, forskere ved OHSU i Portland, Oregon, genereret en tredimensionel model af den humane epitheliale natriumkanal. Kanalen er kritisk til at kontrollere blodtrykke -
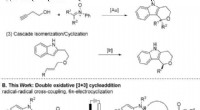 Forskere løfter sløret for en spændende ny måde at producere farmaceutiske ingredienser billiger…Tidligere udviklede syntetiske metoder og bioaktive [2, 3]‐sammensmeltede indoler. Kredit:Professor Cheol-Min Park, UNIST Et forskerhold, tilknyttet Sydkoreas Ulsan National Institute of Science a
Forskere løfter sløret for en spændende ny måde at producere farmaceutiske ingredienser billiger…Tidligere udviklede syntetiske metoder og bioaktive [2, 3]‐sammensmeltede indoler. Kredit:Professor Cheol-Min Park, UNIST Et forskerhold, tilknyttet Sydkoreas Ulsan National Institute of Science a


