Hvordan ændres koboltchlorid med vand?
Farveændringen:
* vandfri koboltchlorid (COCL 2 ): I sin vandfri form (uden vand) er koboltchlorid et blåt pulver.
* Hydreret koboltchlorid (COCL 2 · 6H 2 O): Når det udsættes for vand, absorberer koboltchlorid vandmolekyler og danner et lyserødt hydrat, COCL 2 · 6H 2 O. Denne ændring er reversibel.
Den kemiske reaktion:
Farveændringen skyldes en ændring i koordinationsmiljøet omkring koboltionen (CO 2+ ).
* vandfri: I den vandfri form er koboltionen omgivet af chloridioner (cl - ), giver den en blå farve.
* hydreret: Når der er vand, danner koboltionen koordinationsbindinger med vandmolekyler, der erstatter chloriderne. Vandmolekylerne omkring koboltionen skaber et andet koordinationsmiljø, hvilket fører til den lyserøde farve.
Faktorer, der påvirker farveændringen:
* Vandkoncentration: Jo mere vand er til stede, jo mere hydreret bliver koboltchloridet, hvilket fører til en dybere lyserød farve.
* Temperatur: Farveændringen er mere markant ved højere temperaturer på grund af øget vandabsorption.
* Fugtighed: Koboltchlorid kan også ændre farve i fugtige miljøer på grund af absorptionen af vanddamp fra luften.
Ansøgninger:
Denne farveændringsegenskab gør koboltchlorid nyttigt i forskellige anvendelser:
* fugtighedsindikatorer: Koboltchloridpapir bruges som en simpel fugtighedsindikator, der skifter farve fra blå til lyserød i nærvær af vand.
* Kemiske indikatorer: Det bruges som en indikator i kemiske reaktioner for at signalere tilstedeværelsen eller fraværet af vand.
* tørremiddel (tørringsmiddel): Dets evne til at absorbere vand gør det nyttigt som et tørringsmiddel i visse industrielle anvendelser.
Vigtig note: Cobaltchlorid er et giftigt kemikalie. Det skal håndteres med omhu, og passende sikkerhedsforholdsregler skal træffes.
Sidste artikelHvad er den afbalancerede ligning for cæsium og klor?
Næste artikelEn formel bruges til at repræsentere hvad i kemi?
 Varme artikler
Varme artikler
-
 Billig vandbehandlingDe nye nikkelkatalysatorer syntetiseret ved Institute of Physical Chemistry PAS muliggør ekstremt effektiv vandbehandling i flowtilstand, der fjerner skadelige organoklorforbindelser. Kredit:IPC PAS,
Billig vandbehandlingDe nye nikkelkatalysatorer syntetiseret ved Institute of Physical Chemistry PAS muliggør ekstremt effektiv vandbehandling i flowtilstand, der fjerner skadelige organoklorforbindelser. Kredit:IPC PAS, -
 Forskere udvikler ny teknologi til udvinding af ikke-jernholdige og ædle metallerKredit:Ural Federal University Forskere ved Ruslands Ural Federal University (UrFU) arbejder på at løse problemet med at udvinde ikke-jernholdige og ædle metaller, som findes i malme, der er svære
Forskere udvikler ny teknologi til udvinding af ikke-jernholdige og ædle metallerKredit:Ural Federal University Forskere ved Ruslands Ural Federal University (UrFU) arbejder på at løse problemet med at udvinde ikke-jernholdige og ædle metaller, som findes i malme, der er svære -
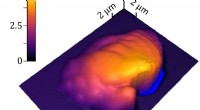 Ny metode måler 3-D polymerbearbejdning præcistEt 3D topografisk billede af en enkelt voxel af polymeriseret harpiks, omgivet af flydende harpiks. NIST-forskere brugte deres sample-coupled-resonance photo-rheology (SCRPR) teknik til at måle, hvord
Ny metode måler 3-D polymerbearbejdning præcistEt 3D topografisk billede af en enkelt voxel af polymeriseret harpiks, omgivet af flydende harpiks. NIST-forskere brugte deres sample-coupled-resonance photo-rheology (SCRPR) teknik til at måle, hvord -
 Giftforskning kan give behandling af mave-tarmsygdommeTerapeutik inspireret af gifte kan være nøglen til behandling af en almindelig mave-tarmsygdom. Kredit:University of Queensland Terapeutik inspireret af gifte kan være nøglen til behandling af en
Giftforskning kan give behandling af mave-tarmsygdommeTerapeutik inspireret af gifte kan være nøglen til behandling af en almindelig mave-tarmsygdom. Kredit:University of Queensland Terapeutik inspireret af gifte kan være nøglen til behandling af en
- Cellelegemer af sensoriske neuroner findes hvor?
- Identificering af prioriteter for at udnytte smarte digitale teknologier til bæredygtig afgrødepro…
- Hvad er Newtons tredje bevægelse?
- Som flygtningelejre svulmer op, Projektet har til formål at bringe toiletter ind i de enkelte hjem
- Hvilke miljøfaktorer får sten til at undergå metamorfe?
- Er Jupiter den største planet i solsystemet?


