Molekonceptet er vigtigt i kemi, fordi?
1. Tilvejebringelse af en konsekvent enhed til måling af stof:
- Det definerer en bestemt mængde stof, ligesom et dusin repræsenterer 12 genstande.
- En mol indeholder altid 6,022 x 10^23 partikler (atomer, molekyler, ioner osv.), Der sikrer en standardiseret måde at sammenligne mængder af forskellige stoffer på.
2. Vedrørende masse, mol og antal partikler:
- Mole forbinder den makroskopiske verden (gram) til den mikroskopiske verden (atomer og molekyler).
- Ved hjælp af molmasse (gram pr. Mol) kan vi nemt konvertere mellem masse og mol, hvilket muliggør beregninger, der involverer kemiske reaktioner.
3. Letter støkiometri:
- Kemiske reaktioner forekommer i specifikke molforhold.
- Molekonceptet giver os mulighed for at forudsige mængderne af reaktanter og produkter, der er involveret i en reaktion, hvilket muliggør nøjagtige beregninger og forudsigelser.
4. Forståelse af koncentrationer og løsninger:
- Molaritet (mol pr. Liter) er en nøgleenhed til at udtrykke koncentrationen af opløsninger.
- Forståelse af moler tillader præcise målinger og kontrol over kemiske reaktioner i opløsninger.
5. Tilslutning af atommasser til praktiske anvendelser:
- Molekonceptet forbinder atommasser (baseret på carbon-12) til masserne af stoffer, vi bruger i laboratoriet.
- Dette gør det muligt for os at beregne masserne af specifikke kemikalier, der kræves til eksperimenter eller industrielle processer.
I det væsentlige fungerer molekonceptet som en bro mellem den teoretiske verden af atomer og molekyler og den praktiske verden af kemiske reaktioner og målinger. Det giver et konsistent og kraftfuldt værktøj til forståelse og manipulering af stof på både mikroskopiske og makroskopiske niveauer.
 Varme artikler
Varme artikler
-
 Gennembrud i forståelsen af enzymer, der laver antibiotika til lægemiddelresistent patogenProf Józef Lewandowski udfører nuklear magnetisk resonansspektroskopi, en nøgleteknikker brugt i arbejdet. Kredit:University of Warwick En af WHOs tre kritiske prioriterede patogener, Acinetobacte
Gennembrud i forståelsen af enzymer, der laver antibiotika til lægemiddelresistent patogenProf Józef Lewandowski udfører nuklear magnetisk resonansspektroskopi, en nøgleteknikker brugt i arbejdet. Kredit:University of Warwick En af WHOs tre kritiske prioriterede patogener, Acinetobacte -
 Kemikere syntetiserer ultrahurtig cyaniddetektorKredit:CC0 Public Domain Organiske kemikere ved Kaunas University of Technology (KTU), Litauen har syntetiseret et nyt materiale, som kan bruges som en detektor for cyanider i vand. Ved kontakt me
Kemikere syntetiserer ultrahurtig cyaniddetektorKredit:CC0 Public Domain Organiske kemikere ved Kaunas University of Technology (KTU), Litauen har syntetiseret et nyt materiale, som kan bruges som en detektor for cyanider i vand. Ved kontakt me -
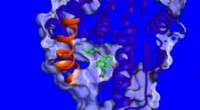 Et spørgsmål om mobilitet:Tværfagligt papir foreslår ny strategi for lægemiddelopdagelseForskelle i strukturen og dynamikken i den spiralformede region (vist i orange) af HSP90-proteinet. Kredit:Heidelberg Institut for Teoretiske Studier En fælles industri/akademiske undersøgelse af
Et spørgsmål om mobilitet:Tværfagligt papir foreslår ny strategi for lægemiddelopdagelseForskelle i strukturen og dynamikken i den spiralformede region (vist i orange) af HSP90-proteinet. Kredit:Heidelberg Institut for Teoretiske Studier En fælles industri/akademiske undersøgelse af -
 Forskere opfinder lette flydende metalmaterialerFigur 1. GB-eGaIn. Kredit:LIU Jing Flydende metal ved stuetemperatur, for eksempel Gallium-baseret legering, har høj elektrisk og termisk ledningsevne, og fremragende flydende. De kan bruges inden
Forskere opfinder lette flydende metalmaterialerFigur 1. GB-eGaIn. Kredit:LIU Jing Flydende metal ved stuetemperatur, for eksempel Gallium-baseret legering, har høj elektrisk og termisk ledningsevne, og fremragende flydende. De kan bruges inden
- Hvad ville der være sket med gassen, hvis molekylære kollisioner ikke var elastiske?
- Boeing ScanEagle opnår det første europæiske luftshow
- Ny stofbelægning kunne forhindre kemiske våben, redde liv
- Bøjning - men ikke brud - på jagt efter nyt materiale
- Er en kvaternær struktur polypeptidsekvens af aminosyrer?
- Computere hjælper med at opdage nye, billigt materiale til at lave LED'er med høj farvekvalitet


