Hvilken forbindelse er farveløs i en vandopløsning Al2SO43 CR2SO43 Fe2SO43 CO2SO43?
* Forståelse af farve i løsninger: Overgangsmetalioner (elementer i D-blokken i den periodiske tabel) danner ofte farvede opløsninger på grund af absorption og emission af lys, når elektroner overgår mellem energiniveauet.
* Forbindelserne:
* al₂ (so₄) ₃: Aluminium (AL) er et gruppe 3 -element, ikke et overgangsmetal. Dens ioner er typisk farveløse.
* cr₂ (so₄) ₃: Krom (CR) er et overgangsmetal. Krom (III) -ioner (cr³⁺) er kendt for deres grønne farve i opløsning.
* fe₂ (so₄) ₃: Jern (Fe) er et overgangsmetal. Jern (III) -ioner (Fe³⁺) kan danne gule til rødbrune opløsninger.
* co₂ (so₄) ₃: Cobalt (CO) er et overgangsmetal. Cobalt (II) -ioner (CO²⁺) er typisk lyserøde eller blå i opløsning, og kobolt (III) -ioner (co³⁺) kan være forskellige farver afhængigt af ligandkoordinationen.
Konklusion:
Derfor er forbindelsen, der er farveløs i en vandopløsning, al₂ (so₄) ₃ .
Sidste artikelHvor mange atomer er der i 0,575 gram cesium?
Næste artikelHvor mange iltatomer er der i denne formel Al2SO43?
 Varme artikler
Varme artikler
-
 Ny metode til fremstilling af prækursorer til højstyrke kulfiberforarbejdningDet kan bruges til at producere kulfiber med nye forbedrede egenskaber. Kredit:Lobachevsky University Kulfiber er et vigtigt strukturelt materiale. På grund af sin høje styrke, i kombination med l
Ny metode til fremstilling af prækursorer til højstyrke kulfiberforarbejdningDet kan bruges til at producere kulfiber med nye forbedrede egenskaber. Kredit:Lobachevsky University Kulfiber er et vigtigt strukturelt materiale. På grund af sin høje styrke, i kombination med l -
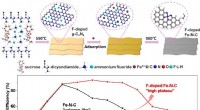 Forskere bruger fluor-dopingmetode til at konstruere katalysatorer med forbedret ydeevneDen F-dopede Fe-N-C enkeltstedskatalysator bevarer fordelen ved lavt overpotentiale for Fe-N-C med meget øget CO faradaisk effektivitet og delvis strømtæthed på grund af den stabiliserede Fe3+ aktive
Forskere bruger fluor-dopingmetode til at konstruere katalysatorer med forbedret ydeevneDen F-dopede Fe-N-C enkeltstedskatalysator bevarer fordelen ved lavt overpotentiale for Fe-N-C med meget øget CO faradaisk effektivitet og delvis strømtæthed på grund af den stabiliserede Fe3+ aktive -
 Kemikere opfinder en ny Lewis surhedstest ved hjælp af fluorescensKredit:York University York University kemikere har opfundet en ny fluorescens-baseret metode til nøjagtigt at bestemme styrken af en række Lewis-syrer, som en dag kunne bruges til at hjælpe med
Kemikere opfinder en ny Lewis surhedstest ved hjælp af fluorescensKredit:York University York University kemikere har opfundet en ny fluorescens-baseret metode til nøjagtigt at bestemme styrken af en række Lewis-syrer, som en dag kunne bruges til at hjælpe med -
 Ingeniører bruger varmefri teknologi til fleksibel elektronik, tryk metal på blomster, gelatineMartin Thuo og hans forskergruppe har udviklet varmefri teknologi, der kan printe ledende, metalliske linjer og spor på næsten alt, inklusive et rosenblad. Kredit:Martin Thuo. Martin Thuo fra Iowa
Ingeniører bruger varmefri teknologi til fleksibel elektronik, tryk metal på blomster, gelatineMartin Thuo og hans forskergruppe har udviklet varmefri teknologi, der kan printe ledende, metalliske linjer og spor på næsten alt, inklusive et rosenblad. Kredit:Martin Thuo. Martin Thuo fra Iowa
- Hvornår var Laast -tiden, vi besøgte måne?
- Hvilke fire planeter er kendt som gasgiganterne?
- Bånd af rock havbunden, der viser skiftende magnetisk orientering, indikerer, at feltet har?
- Royal Caribbean henter verdens største krydstogtskib
- UK Guardian grupper digitale indtægter overgår print
- Kepler-data afslører eksistensen af 20 lovende exoplaneter, der gemmer sig i almindeligt syn


