Hvad indikerer reaktionshastigheden om en bestemt kemisk reaktion?
* hvor hurtigt koncentrationen af reaktanter falder over tid.
* hvor hurtigt koncentrationen af produkter stiger over tid.
Her er en oversigt over, hvad en høj eller lav reaktionshastighed betyder:
Høj reaktionshastighed:
* Reaktanter forbruges hurtigt, og produkter dannes hurtigt.
* Reaktionen betragtes som hurtig .
Lav reaktionshastighed:
* Reaktanter konsumeres langsomt, og produktdannelsen er langsom.
* Reaktionen betragtes som langsom .
faktorer, der påvirker reaktionshastighed:
* Koncentration af reaktanter: Højere koncentration fører til hyppigere kollisioner og en hurtigere hastighed.
* Temperatur: Højere temperatur øger molekylernes kinetiske energi, hvilket fører til hyppigere og effektive kollisioner, og dermed en hurtigere hastighed.
* overfladeareal: Forøget overfladeareal af faste reaktanter giver mulighed for flere kontaktpunkter, hvilket øger reaktionshastigheden.
* katalysator: Katalysatorer giver en alternativ reaktionsvej med lavere aktiveringsenergi, der fremskynder reaktionen.
Betydningen af reaktionshastighed:
* Forudsigelse af reaktionstid: At kende hastigheden hjælper med at estimere, hvor lang tid en reaktion vil tage at gennemføre.
* Optimering af industrielle processer: Industrier bruger reaktionshastighedsdata til at kontrollere reaktionsbetingelserne for maksimal effektivitet og produktudbytte.
* Forståelse af kemiske mekanismer: Reaktionshastighedsdata hjælper forskere med at studere trinene involveret i en reaktion og bestemme mekanismen.
* Design af nye materialer og reaktioner: At forstå reaktionshastigheder er afgørende for at udvikle nye materialer og processer.
Sammenfattende er reaktionshastigheden et afgørende aspekt ved at forstå kemiske reaktioner og bruges vidt inden for forskellige videnskabelige og industrielle områder.
 Varme artikler
Varme artikler
-
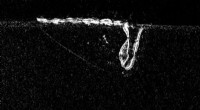 Sprængning af dine (små) bobler:ny forskning peger på vejen mod porefri 3D-printDette røntgenbillede taget ved APS viser en lasersmeltende aluminium under den additive fremstillingsproces. Til venstre for laseren kan du se små porer skabt under processen, som over tid kan skabe f
Sprængning af dine (små) bobler:ny forskning peger på vejen mod porefri 3D-printDette røntgenbillede taget ved APS viser en lasersmeltende aluminium under den additive fremstillingsproces. Til venstre for laseren kan du se små porer skabt under processen, som over tid kan skabe f -
 Katalysator omdanner plastaffald til værdifulde ingredienser ved lav temperaturKredit:Osaka City University For første gang, forskere har brugt en ny katalysatorproces til at genbruge en type plastik, der findes i alt fra indkøbsposer og fødevareemballage til legetøj og elek
Katalysator omdanner plastaffald til værdifulde ingredienser ved lav temperaturKredit:Osaka City University For første gang, forskere har brugt en ny katalysatorproces til at genbruge en type plastik, der findes i alt fra indkøbsposer og fødevareemballage til legetøj og elek -
 For fotokatalysatorer, at klare tidens tand betyder at finde en perfekt partnerKredit:Pixabay/CC0 Public Domain Nøglen til effektivt at høste energi fra sollys kunne være at finde de rigtige kombinationer af lysfangende materialer. Forskere ved KAUST har opdaget, at en form
For fotokatalysatorer, at klare tidens tand betyder at finde en perfekt partnerKredit:Pixabay/CC0 Public Domain Nøglen til effektivt at høste energi fra sollys kunne være at finde de rigtige kombinationer af lysfangende materialer. Forskere ved KAUST har opdaget, at en form -
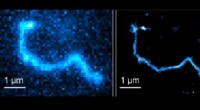 Nye træk for polymerkædedynamikSuperopløsnings fluorescensmikroskopi (højre) giver betydeligt skarpere billeder sammenlignet med konventionel fluorescensmikroskopi. Kredit:Abadi et al. En teknik, der gør det muligt for forskere
Nye træk for polymerkædedynamikSuperopløsnings fluorescensmikroskopi (højre) giver betydeligt skarpere billeder sammenlignet med konventionel fluorescensmikroskopi. Kredit:Abadi et al. En teknik, der gør det muligt for forskere
- Endelig grænse:Rusland udvikler vaskemaskine til plads
- Iagttagelse og eksperimentering er to måder, hvorpå økologer kan besvare videnskabelige spørgsmå…
- Fermi fanger gammaglimt fra tropiske storme
- Polymer nanopartikel overvinder anticancer-lægemiddelresistens
- Pixel 3:En tur til maskinlæring for at få dybdeestimater
- Hvorfor bliver sukkervand fremstillet til kolibrier tåget?


