Hvordan forklarer du ændringen fra fast stof til gas, der ser mellem elementer kulstof og nitrogen?
Her er en sammenbrud:
* carbon: Carbonatomer danner stærke kovalente bindinger med hinanden, hvilket fører til dannelse af store, komplekse strukturer som grafit og diamant. Disse strukturer holdes sammen af stærke kovalente obligationer , som kræver meget energi for at bryde. Derfor har kulstof et højt smeltepunkt og eksisterer som et fast stof ved stuetemperatur.
* nitrogen: Nitrogenatomer danner en tredobbelt binding med hinanden for at danne et diatomisk molekyle (N 2 ). Denne tredobbelte binding er meget stærk, men de intermolekylære kræfter mellem forskellige nitrogenmolekyler er svage van der Waals Forces . Disse kræfter er meget svagere end de kovalente bindinger i nitrogenmolekylet. Som et resultat kan nitrogenmolekyler let overvinde disse svage kræfter ved stuetemperatur, så det kan eksistere som en gas.
Kortfattet:
* stærke kovalente bindinger i kulstofstrukturen føre til en fast tilstand ved stuetemperatur.
* svage intermolekylære kræfter mellem nitrogenmolekyler Lad det eksistere som en gas ved stuetemperatur.
Denne forskel i intermolekylære kræfter er den vigtigste årsag til forskellen i stoftilstande mellem kulstof og nitrogen ved stuetemperatur.
 Varme artikler
Varme artikler
-
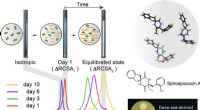 Bestemmelse af atomstrukturen af naturlige produkter hurtigere og mere præcistMåling af den resterende kemiske skiftanisotropi i et flydende krystallinsk medium. Metoden blev brugt til at bestemme stereokemien af spiroepicoccin A, et nyligt opdaget naturprodukt. Det nye natur
Bestemmelse af atomstrukturen af naturlige produkter hurtigere og mere præcistMåling af den resterende kemiske skiftanisotropi i et flydende krystallinsk medium. Metoden blev brugt til at bestemme stereokemien af spiroepicoccin A, et nyligt opdaget naturprodukt. Det nye natur -
 Konvertering af CO2 til lagring af vedvarende energiYuvraj Birdja omdannede CO2 til myresyre for at lagre energi på en bæredygtig måde, med forskellige katalysatorer. Med denne nye viden, forskere er et skridt nærmere i industriel omdannelse af CO2 til
Konvertering af CO2 til lagring af vedvarende energiYuvraj Birdja omdannede CO2 til myresyre for at lagre energi på en bæredygtig måde, med forskellige katalysatorer. Med denne nye viden, forskere er et skridt nærmere i industriel omdannelse af CO2 til -
 Udvikling af cellulær membran-FET (lipid-FET) til følsomhed af biosensorUdfordringer til potentiometriske måleordninger til molekylær detektion på en FET under ionisk miljø:dannelse af EDL, uspecifik binding, og tilfældigt orienterede receptorer. Kredit:Korea Institute of
Udvikling af cellulær membran-FET (lipid-FET) til følsomhed af biosensorUdfordringer til potentiometriske måleordninger til molekylær detektion på en FET under ionisk miljø:dannelse af EDL, uspecifik binding, og tilfældigt orienterede receptorer. Kredit:Korea Institute of -
 Hvordan stabilisering af forstyrrede proteiner kan føre til den næste generation af medicinske app…LCST IDPPer udviser en bred vifte af hysteretisk faseadfærd. (A) Analyse af den reversible faseadfærd af LCST IDPPer i vores bibliotek afslørede tre grupper af gentagne motiver, hvor motiver i hver gr
Hvordan stabilisering af forstyrrede proteiner kan føre til den næste generation af medicinske app…LCST IDPPer udviser en bred vifte af hysteretisk faseadfærd. (A) Analyse af den reversible faseadfærd af LCST IDPPer i vores bibliotek afslørede tre grupper af gentagne motiver, hvor motiver i hver gr
- Kunne usynlige rumvæsener virkelig eksistere blandt os? En astrobiolog forklarer
- Professor foreslår, hvordan et sort hul i kredsløb om planeten kunne være tegn på en avanceret c…
- Hvad er elektronegativiteten af o2?
- Hvilke oplysninger bruger en videnskabsmand til at bestemme en organismer fylogeni?
- Afdækning af hemmelighederne bag ultralavfrekvente gravitationsbølger
- Dannelse af magmahav på eksoplanet


