Hvilket har et større antal atomer et gram helium eller neon?
forståelse af konceptet
* mol og atomer: Antallet af atomer i et stof er direkte proportionalt med antallet af mol. En mol af ethvert stof indeholder Avogadros antal partikler (6,022 x 10^23).
* molmasse: Den molære masse af et element er massen af en mol af dette element.
Beregninger
1. molmasse:
* Helium (HE):4,00 g/mol
* Neon (NE):20,18 g/mol
2. mol i 1 gram:
* Helium:(1 g) / (4,00 g / mol) =0,25 mol
* Neon:(1 g) / (20,18 g / mol) =0,049 mol
3. Antal atomer:
* Helium:(0,25 mol) * (6,022 x 10^23 atomer/mol) =1,51 x 10^23 atomer
* Neon:(0,049 mol) * (6,022 x 10^23 atomer/mol) =2,95 x 10^22 atomer
Konklusion
Et gram helium Indeholder et større antal atomer end et gram neon.
 Varme artikler
Varme artikler
-
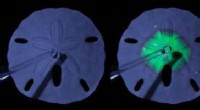 Fra søpindsvinskelet til solcellerDenne billedserie viser et skelet med sanddollar, der gradvist konverterer til en lysemitterende perovskit. Snapshots af denne konvertering er taget på 0s, 5s, 15erne, og 40erne. Kredit:Noorduin Lab,
Fra søpindsvinskelet til solcellerDenne billedserie viser et skelet med sanddollar, der gradvist konverterer til en lysemitterende perovskit. Snapshots af denne konvertering er taget på 0s, 5s, 15erne, og 40erne. Kredit:Noorduin Lab, -
 Team opnår to-elektron kemiske reaktioner ved hjælp af lysenergi, guldUnder de rette forhold, guld nanopartikler absorberer lys og overfører elektroner til andre reaktanter. Denne proces kan bruges til at omdanne CO2 og vand til kulbrinter. I grafikken, kulstofatomer er
Team opnår to-elektron kemiske reaktioner ved hjælp af lysenergi, guldUnder de rette forhold, guld nanopartikler absorberer lys og overfører elektroner til andre reaktanter. Denne proces kan bruges til at omdanne CO2 og vand til kulbrinter. I grafikken, kulstofatomer er -
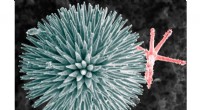 Nærmere kig afslører aksiale filamenter i havsvampspikler, der består af proteinerElektronmikroskopibillede af glasspikler fra svampen Geodia cydonium. Kredit:Zlotnikov Group, B TERNING, TU Dresden Et team af forskere med medlemmer fra Frankrig, Tyskland og Israel har fundet ud
Nærmere kig afslører aksiale filamenter i havsvampspikler, der består af proteinerElektronmikroskopibillede af glasspikler fra svampen Geodia cydonium. Kredit:Zlotnikov Group, B TERNING, TU Dresden Et team af forskere med medlemmer fra Frankrig, Tyskland og Israel har fundet ud -
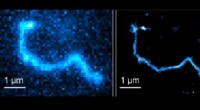 Nye træk for polymerkædedynamikSuperopløsnings fluorescensmikroskopi (højre) giver betydeligt skarpere billeder sammenlignet med konventionel fluorescensmikroskopi. Kredit:Abadi et al. En teknik, der gør det muligt for forskere
Nye træk for polymerkædedynamikSuperopløsnings fluorescensmikroskopi (højre) giver betydeligt skarpere billeder sammenlignet med konventionel fluorescensmikroskopi. Kredit:Abadi et al. En teknik, der gør det muligt for forskere
- Hvilken organelle indeholder fordøjelsesenzymer og hjælper med at fordøje affald inde i cellen?
- Hjerneundersøgelse afslører, hvordan insekter gør sig lige til hjemmet
- Hvad er hastigheden på en bølge, der har frekvens 200 Hz og bølgelængde 2,5 meter?
- Sådan fungerer Occams Razor
- Har Thomas Alva Edison opfandt nogen kredsløb?
- Ben op for fodterapistuderende, da 3-D-printede fødder sætter dem skridt foran resten


