Hvordan opnår ikke -metaller den ædle gaskonfiguration?
* ædle gaskonfiguration: Noble gasser er ekstremt stabile på grund af deres fulde yderste elektronskaller. Derfor er de ureaktive.
* ikke -metal tendens: Ikke -metaller med deres høje elektronegativitet har en tendens til at tiltrække elektroner. Dette gør dem gode til at få elektroner til at blive mere stabile.
* aniondannelse: Når en ikke -metal vinder elektroner, bliver det en negativt ladet ion kaldet en anion. Denne negativt ladede ion har en fuld ydre skal, der ligner konfigurationen af den nærmeste ædle gas.
Eksempler:
* klor (Cl): Klor har 7 valenselektroner. Det får en elektron for at opnå konfigurationen af argon (AR), der har 8 valenselektroner. Dette danner chloridion (Cl-).
* ilt (O): Oxygen har 6 valenselektroner. Det får to elektroner for at opnå konfigurationen af neon (NE), der har 8 valenselektroner. Dette danner oxidion (O2-).
Nøglepunkter:
* Ikke -metaller danner typisk ioniske bindinger med metaller, hvor de får elektroner fra metallet for at opnå den ædle gaskonfiguration.
* Antallet af elektroner opnået ved en ikke -metal bestemmes af dens position på den periodiske tabel og dens elektronegativitet.
* Opnåelse af den ædle gaskonfiguration er et grundlæggende princip i forståelsen af reaktiviteten af ikke -metaller.
Fortæl mig, hvis du har andre spørgsmål!
Sidste artikelHvorfor giver Platinum atomnummeret 78?
Næste artikelHvilken type reaktion er forbrænding af benzin til frigivelse af energi?
 Varme artikler
Varme artikler
-
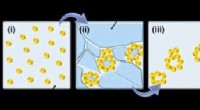 Multi-skala strukturerede materialer til elektrokatalyse og fotoelektrokatalyseSkematisk præsentation af fryse-tø-metoden. Kredit:Wiley-VCH Som en ny klasse af porøse materialer, noble metal aerogels (NMAer) har tiltrukket opmærksomhed for deres selvbærende arkitekturer, høj
Multi-skala strukturerede materialer til elektrokatalyse og fotoelektrokatalyseSkematisk præsentation af fryse-tø-metoden. Kredit:Wiley-VCH Som en ny klasse af porøse materialer, noble metal aerogels (NMAer) har tiltrukket opmærksomhed for deres selvbærende arkitekturer, høj -
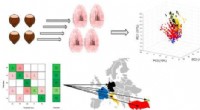 Godkendelse af hasselnøddernes geografiske oprindelseKredit:American Chemical Society Hasselnødder, som olivenolie, ost og andre landbrugsprodukter varierer i smag afhængigt af deres geografiske oprindelse. Fordi forbrugere og processorer er villige
Godkendelse af hasselnøddernes geografiske oprindelseKredit:American Chemical Society Hasselnødder, som olivenolie, ost og andre landbrugsprodukter varierer i smag afhængigt af deres geografiske oprindelse. Fordi forbrugere og processorer er villige -
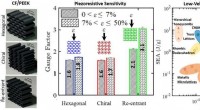 Letvægts, slagfaste bikagestrukturer kan fornemme, når de er blevet beskadigetGrafisk abstrakt. Kredit: Materialer og design (2021). DOI:10.1016/j.matdes.2021.109863 En ny form for letvægts, slagfaste plastbaserede honningkage-strukturer, der kan mærke, hvornår de er bleve
Letvægts, slagfaste bikagestrukturer kan fornemme, når de er blevet beskadigetGrafisk abstrakt. Kredit: Materialer og design (2021). DOI:10.1016/j.matdes.2021.109863 En ny form for letvægts, slagfaste plastbaserede honningkage-strukturer, der kan mærke, hvornår de er bleve -
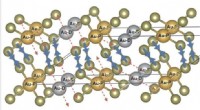 Forskere løser det gyldne puslespil med kalaveritDannelse af Te-Te dimererne på grund af ladningsdisproportionering på Au-steder. Kredit:S. V. Streltsov et al./ PNAS Forskere fra Rusland og Tyskland har kastet lys over den krystallinske strukt
Forskere løser det gyldne puslespil med kalaveritDannelse af Te-Te dimererne på grund af ladningsdisproportionering på Au-steder. Kredit:S. V. Streltsov et al./ PNAS Forskere fra Rusland og Tyskland har kastet lys over den krystallinske strukt
- Hvilke planeter har en tynd atmosfære eller slet ingen?
- Når hyppigheden af kilde en vandbølge øger hastighedsbølgerne, der kører i stigninger. Er det…
- Juli 2019 varmeste måned nogensinde for planeten:NOAA
- Hvad er den molekylære formel for Vineger?
- Forskere finder ud af, at stråling i rummet bliver mere og mere farlig
- Hvor mange asteroider har ramt månen?


