Hvad er den gennemsnitlige translationelle kinetiske energi af gasmolekyler?
ke =(3/2) * k * t
Hvor:
* ke er den gennemsnitlige translationelle kinetiske energi
* k er Boltzmann konstant (1,38 × 10⁻²³ j/k)
* t er den absolutte temperatur i Kelvin
Nøglepunkter:
* translationel kinetisk energi Henviser til energien forbundet med bevægelsen af molekyler fra et punkt til et andet.
* Denne ligning gælder for ideelle gasser, hvor intermolekylære kræfter er ubetydelige.
* Ligningen indebærer, at når temperaturen øges, øges den gennemsnitlige hastighed for gasmolekylerne, og derfor øges den kinetiske energi også.
Eksempel:
Lad os sige, at temperaturen på en gas er 300 K. Derefter ville den gennemsnitlige translationelle kinetiske energi af gasmolekylerne være:
Ke =(3/2) * (1,38 × 10 ²³ J/K) * (300 K)
Ke ≈ 6,21 × 10⁻²¹ j
Bemærk: Den gennemsnitlige translationelle kinetiske energi er en gennemsnitlig værdi. Individuelle gasmolekyler vil have forskellige kinetiske energier, men gennemsnittet vil følge dette forhold til temperatur.
Sidste artikelHvad er den lignende og forskel i elementer forbundet?
Næste artikelHvad var Niels Bohr hovedbidrag til kemi?
 Varme artikler
Varme artikler
-
 Udviklet illusion - den sorteste sort giver paradisfuglen en kantKredit:Ed Scholes Paradisfuglens parringsskærm skylder sin optiske ekstravagance en baggrund så sort, at den misundes af teleskop- og solpanelingeniører, ifølge en ny undersøgelse offentliggjort 9
Udviklet illusion - den sorteste sort giver paradisfuglen en kantKredit:Ed Scholes Paradisfuglens parringsskærm skylder sin optiske ekstravagance en baggrund så sort, at den misundes af teleskop- og solpanelingeniører, ifølge en ny undersøgelse offentliggjort 9 -
 Et usandsynligt ægteskab blandt oxiderClaudia Cancellieri og Sebastian Siol undersøger heterostrukturelle legeringer på Empas Laboratory for Joining Technologies and Corrosion. Kredit:Swiss Federal Laboratories for Materials Science and T
Et usandsynligt ægteskab blandt oxiderClaudia Cancellieri og Sebastian Siol undersøger heterostrukturelle legeringer på Empas Laboratory for Joining Technologies and Corrosion. Kredit:Swiss Federal Laboratories for Materials Science and T -
 Et nyt værktøj til kryo-elektronmikroskopiMikroskopisk billede (øverst) og struktur (nederst) af proteinet hæmocyanin (højre) og tobaksmosaikvirus (til venstre) af iDPC-STEM. Nedenfor de tilsvarende 3D-strukturer ved 3,5 og 6,5 Å opløsning. K
Et nyt værktøj til kryo-elektronmikroskopiMikroskopisk billede (øverst) og struktur (nederst) af proteinet hæmocyanin (højre) og tobaksmosaikvirus (til venstre) af iDPC-STEM. Nedenfor de tilsvarende 3D-strukturer ved 3,5 og 6,5 Å opløsning. K -
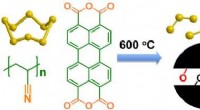 Svovl giver et lovende næste generations batterialternativEn skematisk illustration af dannelsen af kemisk bindingsstabiliseret kulstof-svovlkomposit. Kredit:C. Luo Med den stigende efterspørgsel efter økonomisk overkommelig og bæredygtig energi, den l
Svovl giver et lovende næste generations batterialternativEn skematisk illustration af dannelsen af kemisk bindingsstabiliseret kulstof-svovlkomposit. Kredit:C. Luo Med den stigende efterspørgsel efter økonomisk overkommelig og bæredygtig energi, den l


