Hvad er elektronkonfigurationen af Cu Plus 1?
1. Start med det neutrale kobberatom:
* Kobber (Cu) har et atomnummer på 29, hvilket betyder, at det har 29 protoner og 29 elektroner.
* Elektronkonfigurationen af neutralt kobber er: 1S² 2S² 2P⁶ 3S² 3P⁶ 4S¹ 3D¹⁰ .
* Bemærk den usædvanlige påfyldningsordre:4S -orbitalen udfylder før 3D -orbitalen, men 3D -orbitalen bliver fyldt først, når vi flytter til overgangsmetaller.
2. Konto for +1 -opladningen:
* A +1 ladning betyder, at kobber har mistet en elektron.
* Da 4S -orbitalen er det yderste og højeste energiniveau, er det det elektron, der bliver fjernet.
3. Den endelige elektronkonfiguration af Cu⁺¹:
* 1S² 2S² 2P⁶ 3S² 3P⁶ 3D¹⁰
Fortæl mig, hvis du har andre spørgsmål om elektronkonfiguration!
 Varme artikler
Varme artikler
-
 Video:Sådan interagerer du akavet med mennesker på en bar ved hjælp af kemiKredit:The American Chemical Society Med pandemiske restriktioner ophævet i USA, vi begynder at komme tilbage i verden, mødes med venner og kolleger på restauranter og barer. Hvis du er bekymret,
Video:Sådan interagerer du akavet med mennesker på en bar ved hjælp af kemiKredit:The American Chemical Society Med pandemiske restriktioner ophævet i USA, vi begynder at komme tilbage i verden, mødes med venner og kolleger på restauranter og barer. Hvis du er bekymret, -
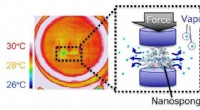 Udvikling af en ny type køling via kraftdrevet flydende gasovergangDen kølende effekt incused af sandwiched nanosvamp. Kredit:Hirotomo Nishihara Et forskerhold fra Tohoku University, Nissan Motor Co., Shinshu Universitet, og Okayama University gjorde en banebryde
Udvikling af en ny type køling via kraftdrevet flydende gasovergangDen kølende effekt incused af sandwiched nanosvamp. Kredit:Hirotomo Nishihara Et forskerhold fra Tohoku University, Nissan Motor Co., Shinshu Universitet, og Okayama University gjorde en banebryde -
 Injektion af fluer med sneglegift kan hjælpe os med at opdage molekyler til udvikling af nye lægem…Kredit:CC0 Public Domain Fluer kunne give en hurtig og billig måde at screene animalsk gift i stor skala for kemikalier, der kan bruges i medicin. Peptider er små kæder af aminosyrer, der udfører
Injektion af fluer med sneglegift kan hjælpe os med at opdage molekyler til udvikling af nye lægem…Kredit:CC0 Public Domain Fluer kunne give en hurtig og billig måde at screene animalsk gift i stor skala for kemikalier, der kan bruges i medicin. Peptider er små kæder af aminosyrer, der udfører -
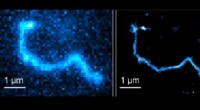 Nye træk for polymerkædedynamikSuperopløsnings fluorescensmikroskopi (højre) giver betydeligt skarpere billeder sammenlignet med konventionel fluorescensmikroskopi. Kredit:Abadi et al. En teknik, der gør det muligt for forskere
Nye træk for polymerkædedynamikSuperopløsnings fluorescensmikroskopi (højre) giver betydeligt skarpere billeder sammenlignet med konventionel fluorescensmikroskopi. Kredit:Abadi et al. En teknik, der gør det muligt for forskere


