Hvad er den molære masse af adrenalin i en opløsning 0,64 g 36,0 CCL4 hæver kogepunktet med 0,49?
forståelse af koncepterne
* kogepunkthøjde: Når et ikke-flygtigt opløst stof (som adrenalin) opløses i et opløsningsmiddel (som CCL4), hæver den kogepunktet for opløsningen. Denne højde er direkte proportional med molaliteten af opløsningen.
* molalitet: Molalitet (M) defineres som molen af opløst stof pr. Kg opløsningsmiddel.
* Ligningen: Forholdet mellem kogepunkthøjde (ΔT B ), molalitet (m) og molal kogepunktforhøjning konstant (k b ) er:
ΔT b =K b * m
trin
1. ) for CCL4: Du skal slå dette op i en referencetabel. K b For CCL4 er ca. 5,02 ° C/m.
2. Beregn molaliteten (M):
* ΔT b =0,49 ° C.
* K b =5,02 ° C/m
* M =ΔT B / K b =0,49 ° C / 5,02 ° C / m =0,0976 m
3. Beregn molen af adrenalin:
* Masse adrenalin =0,64 g
* Masse CCL4 =36,0 g =0,036 kg (konverter gram til kilogram)
* Molalitet =0,0976 mol/kg
* Mol adrenalin =molalitet * Masse opløsningsmiddel =0,0976 mol/kg * 0,036 kg =0,00351 mol
4. Beregn den molære masse:
* Molmasse =masse af adrenalin / mol adrenalin =0,64 g / 0,00351 mol =182,3 g / mol
Derfor er den omtrentlige molære masse af adrenalin i denne opløsning 182,3 g/mol.
Vigtig note: Denne beregning antager, at adrenalin opfører sig ideelt som et ikke-flygtigt opløst stof i CCL4. I virkeligheden kan der være lette afvigelser fra ideel opførsel.
Sidste artikelHvad er de 2 hoveddele af en kemisk ligning?
Næste artikelHvad er opløsningsmidlet og hovedopløsningen i havvand?
 Varme artikler
Varme artikler
-
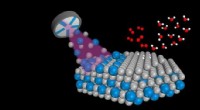 Nanolegeringer 10 gange så effektive som ren platin i brændselscellerNanolegeringer af platin (grå) og yttrium (blå) skabes ved brug af sputtering i et vakuumkammer. Dette gøres ved at rette plasma (lilla) mod et stykke platin med små vedhæftede stykker yttrium. De nan
Nanolegeringer 10 gange så effektive som ren platin i brændselscellerNanolegeringer af platin (grå) og yttrium (blå) skabes ved brug af sputtering i et vakuumkammer. Dette gøres ved at rette plasma (lilla) mod et stykke platin med små vedhæftede stykker yttrium. De nan -
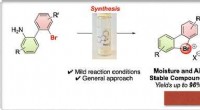 Cykliske hypervalente brom virker som aryne forstadierKredit:Wiley Diaryl λ 3 -bromaner er en sjælden og generelt uforsket klasse af forbindelser. En mild og effektiv protokol leverer nu en bred palet af disse interessante byggesten til organisk sy
Cykliske hypervalente brom virker som aryne forstadierKredit:Wiley Diaryl λ 3 -bromaner er en sjælden og generelt uforsket klasse af forbindelser. En mild og effektiv protokol leverer nu en bred palet af disse interessante byggesten til organisk sy -
 Biller fremkalder udvikling af farveændrende nanopartikler til kommerciel brugOprettelse af farver ved at kopiere billen -nanostrukturer kunne finde applikationer i farvestoffer, blæk og sensorer. Kredit:American Chemical Society Inspireret af de forskellige farver, der ski
Biller fremkalder udvikling af farveændrende nanopartikler til kommerciel brugOprettelse af farver ved at kopiere billen -nanostrukturer kunne finde applikationer i farvestoffer, blæk og sensorer. Kredit:American Chemical Society Inspireret af de forskellige farver, der ski -
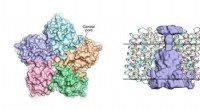 Forskere afslører strukturen af virale rhodopsinerTil venstre:et billede af OLPVRII -pentameren fra den cytoplasmatiske side. Den centrale pore er kontureret af en rød cirkel. Til højre:set fra siden af pentameren. Den centrale pore er farvet lyseb
Forskere afslører strukturen af virale rhodopsinerTil venstre:et billede af OLPVRII -pentameren fra den cytoplasmatiske side. Den centrale pore er kontureret af en rød cirkel. Til højre:set fra siden af pentameren. Den centrale pore er farvet lyseb
- Hvorfor er videnskabsmænd i stand til at forudsige tidevand på forhånd?
- Forskere bruger røntgendiffraktionsmikroskop til at afsløre 3-D indre struktur af hele cellen
- Hvornår er solen direkte over Barbados?
- Elektrontransport i farvestofbaserede solceller
- Orkaner kan føre til modstandsdygtighed - gode nyheder følger dårligt for tropiske skove i Puerto…
- Når menneskelig ekspertise forbedrer maskinernes arbejde


