Natriumchlorid Er leder eller isolator?
solid tilstand:
* ionisk binding: Natriumchlorid er en ionisk forbindelse, hvilket betyder, at det danner et krystalgitter, hvor positivt ladede natriumioner (Na+) og negativt ladede chloridioner (Cl-) holdes sammen af elektrostatiske kræfter.
* faste ioner: I fast tilstand er disse ioner låst i deres positioner inden for gitteret. De kan ikke bevæge sig frit.
* Ingen gratis opladningsbærere: Da ionerne ikke kan flytte, er der ingen gratis ladningsselskaber til at udføre elektricitet. Derfor er fast NaCl en isolator.
opløst i vand eller smeltet:
* ionmobilitet: Når natriumchlorid opløses i vand, dissocieres ionerne (separate) og bliver omgivet af vandmolekyler. Disse opløste ioner kan nu bevæge sig frit.
* opladningsbærere: De mobile ioner i løsningen fungerer som ladningsbærere, hvilket giver elektricitet mulighed for at flyde gennem løsningen.
* Konduktivitet: Derfor er opløst natriumchlorid en god leder af elektricitet. Tilsvarende udfører smeltet NaCl elektricitet, fordi ionerne kan bevæge sig frit i den smeltede tilstand.
Kortfattet: Natriumchloridets evne til at udføre elektricitet afhænger af bevægelsesfriheden for dets ioner. I fast form er ionerne faste og kan ikke bevæge sig, hvilket gør det til en isolator. I opløst eller smeltet form er ionerne frit at bevæge sig, hvilket gør det til en leder.
 Varme artikler
Varme artikler
-
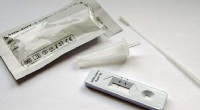 Ny forskning finder måder at forbedre nøjagtigheden af laterale flowtestKredit:Kings College London Forskning offentliggjort i tidsskriftet ACS materialer og grænseflader har givet ny forståelse for, hvordan falsk-negative resultater i laterale flowtest forekommer o
Ny forskning finder måder at forbedre nøjagtigheden af laterale flowtestKredit:Kings College London Forskning offentliggjort i tidsskriftet ACS materialer og grænseflader har givet ny forståelse for, hvordan falsk-negative resultater i laterale flowtest forekommer o -
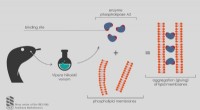 Kemikere opdagede, hvordan hugormegiften virkerKredit:Institut for Bioorganisk Kemi ved Det Russiske Videnskabsakademi Russiske videnskabsmænd rapporterer, at enzymet phospholipase A2 fra Vipera nikolskii-giften er i stand til at klæbe til lip
Kemikere opdagede, hvordan hugormegiften virkerKredit:Institut for Bioorganisk Kemi ved Det Russiske Videnskabsakademi Russiske videnskabsmænd rapporterer, at enzymet phospholipase A2 fra Vipera nikolskii-giften er i stand til at klæbe til lip -
 Supersmøreevne i mikroskala kan bane vejen for fremtidige forbedrede elektromekaniske enhederKredit:CC0 Public Domain Smøreevne måler reduktionen i mekanisk friktion og slid af et smøremiddel. Disse er hovedårsagerne til komponentfejl og energitab i mekaniske og elektromekaniske systemer.
Supersmøreevne i mikroskala kan bane vejen for fremtidige forbedrede elektromekaniske enhederKredit:CC0 Public Domain Smøreevne måler reduktionen i mekanisk friktion og slid af et smøremiddel. Disse er hovedårsagerne til komponentfejl og energitab i mekaniske og elektromekaniske systemer. -
 Teamvidenskab fører til gennembrud inden for kuldioxidomdannelseCharlotte Vogt, Ellen Sterk og Matteo Monai. Kredit:Utrecht University Forskere fra universiteterne i Utrecht og Eindhoven, sammen med kemisk bekymring BASF, har afsløret mekanismen bag CO 2 kon
Teamvidenskab fører til gennembrud inden for kuldioxidomdannelseCharlotte Vogt, Ellen Sterk og Matteo Monai. Kredit:Utrecht University Forskere fra universiteterne i Utrecht og Eindhoven, sammen med kemisk bekymring BASF, har afsløret mekanismen bag CO 2 kon
- Ag-tech kan ændre, hvordan verden spiser
- Sådan fungerer F/A-22 Raptors
- JILAS kort, fleksibel, genanvendelig AFM-sonde
- Løftet om nanofremstilling ved hjælp af DNA-origami
- Forskere opdager, hvordan dødelig svamp beskytter sig selv
- Kunne nyligt spottede dunkle punktkilder forklare det galaktiske centeroverskud (GCE)?


