Hvilken type binding dannes mellem barium og ilt?
Her er hvorfor:
* barium Har to valenselektroner (elektroner i sin yderste skal) og ønsker at miste dem for at opnå en stabil elektronkonfiguration som den ædle gas xenon.
* ilt Har seks valenselektroner og ønsker at få to elektroner for at opnå en stabil elektronkonfiguration som den ædle gas neon.
Når barium og ilt reagerer, mister barium to elektroner for at blive en +2 -kation (Ba²⁺), og ilt får to elektroner til at blive en -2 -anion (O²⁻). Disse modsatte ladede ioner vil derefter tiltrække hinanden og danne en ionisk binding.
Den resulterende forbindelse er bariumoxid (BAO) .
Sidste artikelHvad er et stof, der består af to eller flere elementer, der ikke kombineres kemisk?
Næste artikelNår kemisk binding opstår?
 Varme artikler
Varme artikler
-
 Forskere simulerer processen med klæbende slidComputersimuleringen viser klæbende slid på en selv-affin overflade. Kredit:LSMS / EPFL Overfladeslid beskriver processen med materialetab, når to overflader kommer i kontakt med hinanden. Det har
Forskere simulerer processen med klæbende slidComputersimuleringen viser klæbende slid på en selv-affin overflade. Kredit:LSMS / EPFL Overfladeslid beskriver processen med materialetab, når to overflader kommer i kontakt med hinanden. Det har -
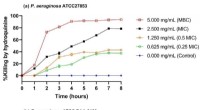 Forbindelse fundet i træer har potentiale til at dræbe lægemiddelresistente bakterierTidsdræbende kurver for (a) lægemiddelfølsom stamme P. aeruginosa ATCC27853 og (b) multilægemiddelresistent stamme P. aeruginosa ATCC BAA-2108 behandlet med og uden indikerede koncentrationer af hydro
Forbindelse fundet i træer har potentiale til at dræbe lægemiddelresistente bakterierTidsdræbende kurver for (a) lægemiddelfølsom stamme P. aeruginosa ATCC27853 og (b) multilægemiddelresistent stamme P. aeruginosa ATCC BAA-2108 behandlet med og uden indikerede koncentrationer af hydro -
 Forskere rapporterer bio-inspirerede selektive antibiotikaSelektive antibiotika muliggør præcisionsindgreb i mikrobiomet (computergrafik). Kredit:Universitetet i Konstanz Da multiresistente bakterier bliver mere og mere en trussel, vi har mere end nogens
Forskere rapporterer bio-inspirerede selektive antibiotikaSelektive antibiotika muliggør præcisionsindgreb i mikrobiomet (computergrafik). Kredit:Universitetet i Konstanz Da multiresistente bakterier bliver mere og mere en trussel, vi har mere end nogens -
 4-D bioingeniørmaterialer bøjning, kurve som naturligt væv4D hydrogel-baserede materialer kan gennemgå flere konformationelle formændringer som reaktion på miljømæssige signaler. Kredit:Aixiang Ding Vævsteknik har længe været afhængig af geometrisk stati
4-D bioingeniørmaterialer bøjning, kurve som naturligt væv4D hydrogel-baserede materialer kan gennemgå flere konformationelle formændringer som reaktion på miljømæssige signaler. Kredit:Aixiang Ding Vævsteknik har længe været afhængig af geometrisk stati
- Hvad er afslutningen på dette ord ligning natrium plus jerncarbonat?
- Grubhub køber LevelUp mobilbestillings- og betalingsselskab for $ 390 millioner
- Hvilken type binding er BrF3?
- Hvilke livsprocesser udfører mikroorganismer?
- Teamet afkræfter hypoteser om perovskit-solceller, hvilket muliggør bedre tilgange til målrettet …
- Uddybende spørgsmål:Er peak oil en myte?


