Hvad er den sammensatte Li3p?
Her er en sammenbrud:
* li: Repræsenterer elementet lithium
* p: Repræsenterer elementets fosfor
* 3: Angiver, at der er tre lithiumatomer for hvert phosphoratom.
egenskaber ved lithiumphosphid:
* udseende: Det er et rødbrunt fast stof.
* reaktivitet: Det er en meget reaktiv forbindelse, især med vand og luft. Det reagerer voldsomt med vand for at producere phosphingas (PH3), hvilket er meget giftigt.
* anvendelser: Lithiumphosphid har begrænsede praktiske anvendelser på grund af dets reaktivitet. Det bruges imidlertid i forskning og som et reagens i visse kemiske reaktioner.
Sikkerhedshensyn:
Lithiumphosphid er en farlig forbindelse og bør håndteres med ekstrem forsigtighed. Det er meget giftigt og brandfarligt. Brug altid passende personligt beskyttelsesudstyr, når du håndterer denne forbindelse og arbejd i et godt ventileret område.
Sidste artikelHvor mange carbonatomer er afbildet i formlen C8H18?
Næste artikelHvilke fire små molekyler er der behov for af levende ting?
 Varme artikler
Varme artikler
-
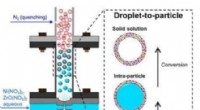 Nanoshell-katalysatorer gør drivhusgasser til nyttige kemikalierEt diagram, der viser, hvordan den nye nikkelbaserede katalysator er skabt ved hjælp af den unikke flammeaerosolproces, der er skabt i Mark Swiharts laboratorium. Kredit:University at Buffalo Et bi
Nanoshell-katalysatorer gør drivhusgasser til nyttige kemikalierEt diagram, der viser, hvordan den nye nikkelbaserede katalysator er skabt ved hjælp af den unikke flammeaerosolproces, der er skabt i Mark Swiharts laboratorium. Kredit:University at Buffalo Et bi -
 Radikalt nyt behandlingssystem lyser op i kræftbehandlingForskere fra Institute of Industrial Science, University of Tokyo har udviklet et strømlinet foto-uncaging-system til fotodynamisk cancerterapi, ved hjælp af en lyspuls til tumorspecifik aktivering af
Radikalt nyt behandlingssystem lyser op i kræftbehandlingForskere fra Institute of Industrial Science, University of Tokyo har udviklet et strømlinet foto-uncaging-system til fotodynamisk cancerterapi, ved hjælp af en lyspuls til tumorspecifik aktivering af -
 Forskere gør fremskridt inden for kontrol af kamæleonlignende materiale til næste generations com…Kredit:Texas A&M University Forskere fra Texas A&M University rapporterer om betydelige fremskridt i deres forståelse og kontrol af et kamæleonlignende materiale, der kan være nøglen til næste gen
Forskere gør fremskridt inden for kontrol af kamæleonlignende materiale til næste generations com…Kredit:Texas A&M University Forskere fra Texas A&M University rapporterer om betydelige fremskridt i deres forståelse og kontrol af et kamæleonlignende materiale, der kan være nøglen til næste gen -
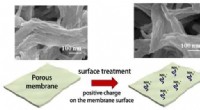 Udvikling af ultratynd holdbar membran til effektiv olie- og vandseparationFigur 1:SEM-billeder og diagram, der viser dannelsen af det ultratynde silicalag på den porøse membran. Kredit:Kobe University Forskere ledet af professor Matsuyama Hideto og professor Yoshioka
Udvikling af ultratynd holdbar membran til effektiv olie- og vandseparationFigur 1:SEM-billeder og diagram, der viser dannelsen af det ultratynde silicalag på den porøse membran. Kredit:Kobe University Forskere ledet af professor Matsuyama Hideto og professor Yoshioka
- Hvad får solens position i himmel og skygger til at ændre sig?
- AI-virksomheden Hypergiant hjælper konsulentfirmaet med at omdanne intellektuel ejendom til produkt…
- Kreativ brug af støj bringer bio-inspireret elektronisk forbedring
- Påvirker positionen i himlen dagslys?
- Flowapparater prøver op til 1500 kemiske reaktioner om dagen
- Advarselsskilte for en orkan


