Hvordan natriumchlorid er et stof, der har lignende egenskaber som og klor, eller det er en helt anden med sine egne unikke egenskaber?
* Kemisk binding: Natrium og klor reagerer på dannelse af en ionisk binding. Dette betyder, at natrium mister et elektron for at blive en positivt ladet ion (Na+), og klor får et elektron til at blive en negativt ladet ion (Cl-). Disse modsatte ladede ioner tiltrækker hinanden stærkt og danner en krystalgitterstruktur.
* Fysiske egenskaber: Natrium og klor er begge stærkt reaktive elementer. Natrium er et blødt, sølvfarvet metal, der reagerer voldsomt med vand. Klor er en grønlig-gul, giftig gas. Natriumchlorid er på den anden side et hvidt, krystallinsk fast stof, der er ikke-toksisk og let opløst i vand.
* Kemiske egenskaber: Natrium og klor har forskellige kemiske egenskaber. Natrium er et stærkt reduktionsmiddel, mens klor er et stærkt oxidationsmiddel. Natriumchlorid er imidlertid en relativt inert forbindelse, der ikke let reagerer med de fleste stoffer.
Sammenfattende er natriumchlorid et helt nyt stof dannet af en kemisk reaktion mellem natrium og klor. Det udviser helt forskellige fysiske og kemiske egenskaber sammenlignet med dens bestanddele elementer på grund af den ioniske binding og den resulterende krystalgitterstruktur.
 Varme artikler
Varme artikler
-
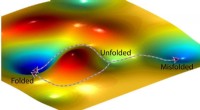 Skjult symmetri fundet i kemiske kinetiske ligningerEn kunstners repræsentation af et landskab med fri energi og to mulige veje, et protein kan følge (venstre) for at folde korrekt og en tredje vej (til højre), der fører til en fejlfoldet tilstand. Kre
Skjult symmetri fundet i kemiske kinetiske ligningerEn kunstners repræsentation af et landskab med fri energi og to mulige veje, et protein kan følge (venstre) for at folde korrekt og en tredje vej (til højre), der fører til en fejlfoldet tilstand. Kre -
 Kortlægning af ændringer i vandmolekylers dynamik og struktur i nærheden af opløste stofferMartina Havenith har hurtigt implementeret den første forskningsidé, som hun ønskede at realisere med midler fra en prestigefyldt bevilling fra Det Europæiske Forskningsråd. Kredit:RUB, Marquard K
Kortlægning af ændringer i vandmolekylers dynamik og struktur i nærheden af opløste stofferMartina Havenith har hurtigt implementeret den første forskningsidé, som hun ønskede at realisere med midler fra en prestigefyldt bevilling fra Det Europæiske Forskningsråd. Kredit:RUB, Marquard K -
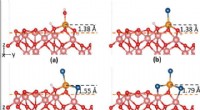 Supercomputermodeller beskriver chlorids rolle i korrosionOverfladestrukturelle ændringer af passive jernfilm forårsaget af adsorption af OH og/eller Cl. (a) Fe (OH) 3, (b) Fe(OH)2Cl, (c) Fe (OH) Cl2, (d) FeCl3. Placeringen af kant-Fe-atomet før adsorption
Supercomputermodeller beskriver chlorids rolle i korrosionOverfladestrukturelle ændringer af passive jernfilm forårsaget af adsorption af OH og/eller Cl. (a) Fe (OH) 3, (b) Fe(OH)2Cl, (c) Fe (OH) Cl2, (d) FeCl3. Placeringen af kant-Fe-atomet før adsorption -
 Første gangs direkte bevis på kemiske reaktioner i partiklerMed denne enhed, partikler kan analyseres bedre end nogensinde før. Kredit:Paul Scherrer Institute/Mahir Dzambegovic Forskere ved Paul Scherrer Institute PSI har udviklet en ny metode til at analy
Første gangs direkte bevis på kemiske reaktioner i partiklerMed denne enhed, partikler kan analyseres bedre end nogensinde før. Kredit:Paul Scherrer Institute/Mahir Dzambegovic Forskere ved Paul Scherrer Institute PSI har udviklet en ny metode til at analy
- Molybdæn titanium carbid levedygtig i additiv fremstilling
- Hvilke betingelser kræves for en solcellypse?
- I astronomi er der blå giganter, har de navne eller bare kaldet rød osv.?
- Den mexicanske regering siger, at tog ikke udgør nogen trussel mod skelettet
- Findes Higgs-bosonen?
- Hvor store oversvømmelser og kompleks infrastruktur kunne have udløst gamle Angkors død


