Hvad er så specielt ved kulstofforbindelser, at de afsatte en hel gren af kemi til den?
1. Alsidighed og bindingsfunktioner:
* Fire valenselektroner: Carbon har fire valenselektroner, hvilket giver det mulighed for at danne fire kovalente bindinger med andre atomer. Denne unikke funktion gør det muligt for kulstof at binde med sig selv og en bred vifte af andre elementer, hvilket skaber en forbløffende mangfoldighed af molekyler.
* Stærke kulstof-carbonbindinger: Carbonatomer kan danne stærke enkelt-, dobbelt- og tredobbeltbindinger med hinanden og skabe kæder, ringe og indviklede strukturer af varierende kompleksitet.
* tetrahedral geometri: Carbon's fire bindinger er arrangeret i en tetrahedral geometri, der påvirker molekylernes form og egenskaber.
2. Livets byggesten:
* organiske molekyler: Carbon er den grundlæggende byggesten for alle kendte livsformer.
* Biomolekyler: Carbohydrater, lipider, proteiner og nukleinsyrer (DNA og RNA) er alle kulstofbaserede molekyler, der er essentielle for livsprocesser.
* makromolekyler: Carbon kan danne store komplekse molekyler kendt som makromolekyler, der spiller vigtige roller i biologiske systemer.
3. Diverse funktionalitet og egenskaber:
* Funktionelle grupper: Forskellige arrangementer af atomer og bindinger, kaldet funktionelle grupper, kan fastgøres til kulstofryggener. Dette skaber en lang række molekyler med forskellige egenskaber, der spænder fra brændstof til farmaceutiske stoffer.
* bred vifte af ejendomme: Kulstofforbindelser udviser en lang række egenskaber, herunder opløselighed, kogepunkt, surhedsgrad og reaktivitet.
* isomerisme: Carbon's bindingsfleksibilitet muliggør forskellige arrangementer af atomer inden for et molekyle (isomerer), hvilket fører til unikke egenskaber og funktioner.
4. Teknologisk betydning:
* polymerer: Syntetiske polymerer som plast, gummier og fibre er kulstofbaserede materialer med brede anvendelser i forskellige brancher.
* Medicin: Et stort flertal af medicin er kulstofbaseret, hvor organisk kemi spiller en afgørende rolle i deres design og syntese.
* brændstoffer og energi: Fossile brændstoffer som kul, olie og naturgas består primært af kulstofforbindelser, hvilket giver energi til vores moderne verden.
I det væsentlige har Carbon's unikke bindingsegenskaber, dens evne til at danne forskellige og komplekse strukturer, og dens rolle i grundlaget for liv har gjort organisk kemi til et uundværligt studiefelt. Forståelsen af kulstofforbindelser er afgørende for at fremme vores viden inden for områder som medicin, materialevidenskab og miljøvidenskab.
Sidste artikelIdentificer et stof, der diffuse frutosetake sted?
Næste artikelHvem har mange elektroner uunpentium?
 Varme artikler
Varme artikler
-
 Hvordan stressede tumorceller undslipper celledød:Ny mekanisme opdagetEn model af et cystein persulfid molekyle. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01145-w En celle dør af ferroptose, når frie radikaler kommer ud af kontrol og ødelægger den
Hvordan stressede tumorceller undslipper celledød:Ny mekanisme opdagetEn model af et cystein persulfid molekyle. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01145-w En celle dør af ferroptose, når frie radikaler kommer ud af kontrol og ødelægger den -
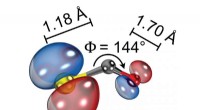 Bestemmelse af strukturen af et molekyle med laserinduceret elektrondiffraktionSkematisk illustration af den molekylære struktur af ioniseret carbonylsulfid (OCS + ) viser dens bøjede og asymmetriske konfiguration og bindingslængderne mellem atomer. Kredit:ICFO Lysmikrosko
Bestemmelse af strukturen af et molekyle med laserinduceret elektrondiffraktionSkematisk illustration af den molekylære struktur af ioniseret carbonylsulfid (OCS + ) viser dens bøjede og asymmetriske konfiguration og bindingslængderne mellem atomer. Kredit:ICFO Lysmikrosko -
 Undersøgelse afslører radikale rynker i dannelsen af komplekse kulstofmolekyler i rummetDette sammensatte billede viser en illustration af en kulstofrig rød kæmpestjerne (midten), der opvarmer en exoplanet (nederst til venstre) og en overlejring af en nyfundet vej, der kunne gøre det mul
Undersøgelse afslører radikale rynker i dannelsen af komplekse kulstofmolekyler i rummetDette sammensatte billede viser en illustration af en kulstofrig rød kæmpestjerne (midten), der opvarmer en exoplanet (nederst til venstre) og en overlejring af en nyfundet vej, der kunne gøre det mul -
 Nyt materiale viser sig at afsalte vand mere effektivtKredit:University of Notre Dame Inden 2025, to tredjedele af verdens befolkning kan opleve mangel på ferskvand. For at løse dette problem, forskere fra University of Notre Dame har identificeret e
Nyt materiale viser sig at afsalte vand mere effektivtKredit:University of Notre Dame Inden 2025, to tredjedele af verdens befolkning kan opleve mangel på ferskvand. For at løse dette problem, forskere fra University of Notre Dame har identificeret e
- Lava, der bevæger sig under jordoverfladen, er hvilken type lavafelt?
- Holdning til mangfoldighed bidrager til at hjælpe flygtninge med at blive produktive medlemmer af e…
- Kirigami inspirerer til ny metode til bærbare sensorer
- Hvordan bestemmer du antallet af elementer, der bruger formel A -forbindelse?
- 3 udbrud af Alaska-vulkaner, der spytter lava- eller askeskyer
- Oversvømmelser er nødvendige for at opretholde sunde flodøkosystemer, forskning viser


