Hvilke kemiske neutraliserer acetone?
Der er dog nogle ting at huske på:
* Vand: Acetone er blandbar med vand, hvilket betyder, at de blandes i enhver andel. Dette "neutraliserer" ikke kemisk acetone, men det kan fortynde det og gøre det mindre potent.
* Stærke baser: Acetone reagerer langsomt med stærke baser som natriumhydroxid (NaOH) for at danne salte. Dette er typisk ikke en neutraliseringsreaktion i klassisk forstand, da det involverer en kemisk ændring.
* Oxidationsmidler: Acetone kan oxideres for at danne andre forbindelser som eddikesyre. Dette er ikke en neutraliseringsreaktion, men snarere en kemisk transformation.
Det er vigtigt at bemærke:
* sikkerhed: Acetone er brandfarlig og bør håndteres med omhu.
* Specifikke applikationer: Den bedste måde at "neutralisere" acetone afhænger af den specifikke anvendelse. For eksempel, hvis du rydder op i et spild, kan vand eller et ikke-brandfarligt opløsningsmiddel være passende.
* konsulter en kemiker: Hvis du har en bestemt anvendelse i tankerne, er det altid den sikreste tilgang at konsultere en kemiker eller et materialesikkerhedsdatablad (MSDS) til acetone.
Fortæl mig, hvis du har en bestemt applikation i tankerne, og jeg kan give mere skræddersyet rådgivning.
Sidste artikelHvorfor bruges FECL2 ikke til at identificere phenol?
Næste artikelEr Bolling Water en kemisk ændring?
 Varme artikler
Varme artikler
-
 Et tidligt advarselssystem for skader i kompositmaterialerDet er første gang, at data er blevet brugt på nationalt plan til at vurdere, hvordan miljøets skønhed påvirker udviklingen af vindmølleparker på land. Kredit:CC0 Public Domain Et hold ved Natio
Et tidligt advarselssystem for skader i kompositmaterialerDet er første gang, at data er blevet brugt på nationalt plan til at vurdere, hvordan miljøets skønhed påvirker udviklingen af vindmølleparker på land. Kredit:CC0 Public Domain Et hold ved Natio -
 Femdobbelt boost i formaldehydudbytteReaktorer, der anvendes til parallel screening af virkningerne af forskellige tryk på formaldehydsyntese. Kredit:O. Trapp Der er et presserende behov for miljøvenlige metoder til industriel produk
Femdobbelt boost i formaldehydudbytteReaktorer, der anvendes til parallel screening af virkningerne af forskellige tryk på formaldehydsyntese. Kredit:O. Trapp Der er et presserende behov for miljøvenlige metoder til industriel produk -
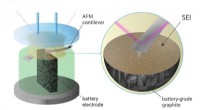 Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p
Forskere får et smugkig på en nøgleproces i batterilevetidenEn hovedoversigt over eksperimentet. Kredit:Pavel Odinev / Skoltech Forskere fra Skoltech Center for Energividenskab og Teknologi (CEST) visualiserede dannelsen af en fast elektrolyt-interfase p -
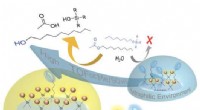 Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me
Nøglebeviser, der forbinder hydrofobicitet med effektiv syrekatalyseForenklet skematisk, der viser, hvordan alkylacetater med lange haler ikke kan nærme sig sure sulfo-steder (blå skiver) i hydrofile miljøer; imidlertid, de kan nærme sig hydrofobe miljøer med flere me
- Hvad er den kemiske formel til at kombinere Ca2 Plus ASO3- 4?
- Er afstanden mellem en poing af en bølge til samme punkt i næste bølge?
- Hvordan man designer et forsøg til at teste, hvordan pH påvirker enzymreaktioner
- Evakuerer 70.000 sportsfans på mindre end en time?
- En blanding, der har en masse opløst stof opløst i den?
- Sådan beregnes luftstrømmen og det statiske trykfald gennem Grill


