Hvilken reaktion er ligevægtskonstanten?
Her er en sammenbrud:
* reversibel reaktion: En kemisk reaktion, hvor produkterne kan reagere for at danne reaktanterne igen.
* ligevægt: Staten, hvor hastighederne for de fremadgående og omvendte reaktioner er ens, og koncentrationerne af reaktanter og produkter forbliver konstante over tid.
ligevægtskonstanten, K, defineres som:
K =(produkter) / (reaktanter)
hvor:
* Produkter: Koncentrationen (eller delvis tryk) af produkterne, der hæves til deres støkiometriske koefficienter i den afbalancerede kemiske ligning.
* reaktanter: Koncentrationen (eller delvist tryk) af reaktanterne hævet til deres støkiometriske koefficienter.
Eksempel:
For reaktionen:
AA + BB ⇌ CC + DD
Ligevægtskonstanten er:
K =([c]^c * [d]^d) / ([a]^a * [b]^b)
Hvad fortæller værdien af k os?
* k> 1: Reaktionen favoriserer dannelsen af produkter i ligevægt. Der vil være flere produkter end reaktanter i ligevægt.
* k <1: Reaktionen favoriserer dannelsen af reaktanter ved ligevægt. Der vil være flere reaktanter end produkter i ligevægt.
* k =1: Reaktionen er afbalanceret, hvilket betyder, at koncentrationen af produkter og reaktanter er omtrent lige med ligevægt.
Vigtige noter:
* Ligevægtskonstanten er en temperaturafhængig mængde.
* Enhederne af K afhænger af den specifikke reaktion og den måde, koncentrationer udtrykkes på.
* K er et kraftfuldt værktøj til at forudsige retningen for en reaktion og omfanget af produktdannelse.
Fortæl mig, hvis du gerne vil have en mere dybdegående forklaring eller specifikke eksempler!
 Varme artikler
Varme artikler
-
 Smart label kunne en dag fortælle dig, hvornår du skal smide mad og kosmetikSmarte etiketter til kosmetik og fødevarer kunne en dag fortælle forbrugerne, hvornår de skal smide et produkt ud. Kredit:Silvana Andreescu Detektering af mad og kosmetisk fordærv og forurening. I
Smart label kunne en dag fortælle dig, hvornår du skal smide mad og kosmetikSmarte etiketter til kosmetik og fødevarer kunne en dag fortælle forbrugerne, hvornår de skal smide et produkt ud. Kredit:Silvana Andreescu Detektering af mad og kosmetisk fordærv og forurening. I -
 Video:Er bakterier fremtiden for olieudslip og oprydning af radioaktivt affald?Kredit:The American Chemical Society Deepwater Horizon-udslippet i 2010 frigav millioner af tons olie i havet. Mens regeringer og olieindustrien forsøgte at rydde op i katastrofen, var bakterier al
Video:Er bakterier fremtiden for olieudslip og oprydning af radioaktivt affald?Kredit:The American Chemical Society Deepwater Horizon-udslippet i 2010 frigav millioner af tons olie i havet. Mens regeringer og olieindustrien forsøgte at rydde op i katastrofen, var bakterier al -
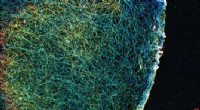 Nye beacons lyser op i interiøretTredimensionel struktur af actin filament netværket i en Cos7 celle, mærket med affimerer og afbildet med DNA-PAINT. Farvekoden angiver niveauerne af filamenterne i cellen (rød:200 nm, blå:-300 nm). M
Nye beacons lyser op i interiøretTredimensionel struktur af actin filament netværket i en Cos7 celle, mærket med affimerer og afbildet med DNA-PAINT. Farvekoden angiver niveauerne af filamenterne i cellen (rød:200 nm, blå:-300 nm). M -
 Ny elektrokatalysator udkonkurrerer platin i produktionen af alkalisk brintDen nye katalysator er et nanostruktureret kompositmateriale sammensat af carbon nanotråde med rutheniumatomer bundet til nitrogen og carbon for at danne aktive steder i carbonmatrixen. Elektronmikros
Ny elektrokatalysator udkonkurrerer platin i produktionen af alkalisk brintDen nye katalysator er et nanostruktureret kompositmateriale sammensat af carbon nanotråde med rutheniumatomer bundet til nitrogen og carbon for at danne aktive steder i carbonmatrixen. Elektronmikros


