Er beryllium en positiv eller negativ ion?
Her er hvorfor:
* Berylliums elektronkonfiguration: Beryllium har et atomnummer på 4, hvilket betyder, at det har 4 protoner og 4 elektroner. Dens elektronkonfiguration er 1S² 2S².
* tendens til at miste elektroner: Beryllium har en relativt lav ioniseringsenergi, hvilket betyder, at det kræver mindre energi at fjerne et elektron fra dets yderste skal. Det har en tendens til at miste sine to valenselektroner (fra 2'erne orbital) for at opnå en stabil elektronkonfiguration som helium (1S²).
* Dannelse af en kation: Når Beryllium mister sine to valenselektroner, danner det en kation med en +2 ladning, skrevet som være²⁺.
Derfor danner beryllium en positiv ion, fordi den mister elektroner for at opnå en stabil elektronisk konfiguration.
 Varme artikler
Varme artikler
-
 Metalisk femleddet ring flytter grænserne for aromaticitetProf. Dr. Robert Kretschmer, professor i uorganisk kemi ved Chemnitz University of Technology, undersøger krystaller foran et diffraktometer. Kredit:Jacob Müller | Chemnitz teknologiske universitet
Metalisk femleddet ring flytter grænserne for aromaticitetProf. Dr. Robert Kretschmer, professor i uorganisk kemi ved Chemnitz University of Technology, undersøger krystaller foran et diffraktometer. Kredit:Jacob Müller | Chemnitz teknologiske universitet -
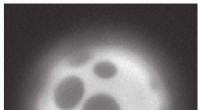 Levende cellemembraner kan selvsortere deres komponenter ved afblandingFaseadskillelse i en syntetisk membran. Kredit:Caitlin Cornell/University of Washington Celler - byggestenene i vores kroppe - er indkapslet af membraner. Det samme gælder de specialiserede rum i
Levende cellemembraner kan selvsortere deres komponenter ved afblandingFaseadskillelse i en syntetisk membran. Kredit:Caitlin Cornell/University of Washington Celler - byggestenene i vores kroppe - er indkapslet af membraner. Det samme gælder de specialiserede rum i -
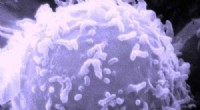 Patientkræftceller vokser pålideligt på nyt 3D-stillads, viser løfte om præcisionsmedicinElektronmikroskopisk billede af en enkelt human lymfocyt. Kredit:Dr. Triche National Cancer Institute En ny 3D-struktur til voksende cellekulturer kan gøre det muligt for læger at teste medicin på
Patientkræftceller vokser pålideligt på nyt 3D-stillads, viser løfte om præcisionsmedicinElektronmikroskopisk billede af en enkelt human lymfocyt. Kredit:Dr. Triche National Cancer Institute En ny 3D-struktur til voksende cellekulturer kan gøre det muligt for læger at teste medicin på -
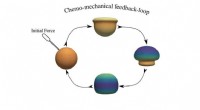 Design af bløde materialer, der efterligner biologiske funktionerKredit:Northwestern University Northwestern Engineering forskere har udviklet en teoretisk model til at designe bløde materialer, der demonstrerer autonome oscillerende egenskaber, der efterligner
Design af bløde materialer, der efterligner biologiske funktionerKredit:Northwestern University Northwestern Engineering forskere har udviklet en teoretisk model til at designe bløde materialer, der demonstrerer autonome oscillerende egenskaber, der efterligner
- Hvad er betydningen af at se en bevægende stjerne på himlen?
- Hvilken plante producerer det mindste frø?
- Hvordan svarer Siri, Google Now på fem spørgsmål
- Sådan hjælper børn med at lære Math Facts
- Hvordan planter justerer fotosyntesen som reaktion på svingende lysintensiteter
- Tyskland klynger sig til diesel, selv da de første kørselsforbud ramte


