Hvad har et opløst stof for at opløses i opløsningsmiddel?
1. "Som opløser som" Princip:
* polære opløste stoffer: Polære opløste stoffer (som sukker eller salt) opløses bedst i polære opløsningsmidler (som vand). Polære molekyler har en positiv og negativ ende på grund af ujævn elektronfordeling. Tiltrækningen mellem de positive og negative ender af opløst stof og opløsningsmiddelmolekyler hjælper dem med at bryde fra hinanden og blandes.
* Ikke-polære opløste stoffer: Ikke-polære opløste stoffer (som olie eller fedt) opløses bedst i ikke-polære opløsningsmidler (som hexan). Ikke-polære molekyler har jævnt fordelt elektroner og har ikke en stærk positiv eller negativ ende. De kan blande godt, fordi de svage attraktioner mellem dem er ens.
2. Intermolekylære kræfter:
* stærkere intermolekylære kræfter: Hvis opløsningen og opløsningsmidlet har stærke intermolekylære kræfter (som hydrogenbinding i vand), kan de interagere effektivt og fremme opløsning.
* svagere intermolekylære kræfter: Hvis kræfterne mellem opløste molekyler er stærkere end kræfterne mellem opløst stof og opløsningsmiddelmolekyler, opløses opløste opløsningsmiddel ikke let.
3. Energiovervejelser:
* entalpi af løsning: Dette er den energiændring, der er forbundet med opløsning. Opløsning kan være enten eksoterm (frigiver varme) eller endotermisk (absorberer varme).
* Entropi af opløsning: Dette er ændringen i lidelse eller tilfældighed under opløsting. Opløsning øger normalt entropi, hvilket gør det gunstigt.
Kortfattet:
* Polaritet: Opløsningen og opløsningsmidlet skal have lignende polaritet.
* Intermolekylære kræfter: Interaktionerne om opløsning af opløsningsmidler skal være stærke nok til at overvinde interaktionerne med opløsning af opløsning og opløsningsmiddel.
* Energi: Enthalpy- og entropiændringerne skal favorisere opløsning.
Fortæl mig, hvis du gerne vil have en mere detaljeret forklaring af nogen af disse punkter!
 Varme artikler
Varme artikler
-
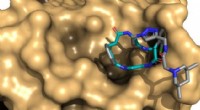 At lære af naturens gavmildhed:Nye biblioteker til lægemiddelopdagelseKunstnerisk skildring af en makrocyklus, der binder til et målprotein. Kredit:Billede:Universitetet i Basel, Basilius Sauter/CC BY-SA 3.0 Naturlige produkter, eller deres nære derivater, lave nogl
At lære af naturens gavmildhed:Nye biblioteker til lægemiddelopdagelseKunstnerisk skildring af en makrocyklus, der binder til et målprotein. Kredit:Billede:Universitetet i Basel, Basilius Sauter/CC BY-SA 3.0 Naturlige produkter, eller deres nære derivater, lave nogl -
 Det værdifulde bidrag fra stress til den termiske stabilitet af nanokornede polykrystallinske leger…Kredit:CC0 Public Domain Nanokornede metaller og legeringer, hvis kornstørrelse er mindre end 100 nm, udviser ekstrem høj styrke og høj duktilitet, har fremragende mekaniske egenskaber. Nanokorned
Det værdifulde bidrag fra stress til den termiske stabilitet af nanokornede polykrystallinske leger…Kredit:CC0 Public Domain Nanokornede metaller og legeringer, hvis kornstørrelse er mindre end 100 nm, udviser ekstrem høj styrke og høj duktilitet, har fremragende mekaniske egenskaber. Nanokorned -
 Krystalklar opløsningsmiddelfiltreringMembranen adskilte effektivt en blanding af to farvestoffer (blå) i dens komponenter, bliver ferskvandsgul. Kredit:The American Chemical Society Kovalente organiske materialer med velordnede porøs
Krystalklar opløsningsmiddelfiltreringMembranen adskilte effektivt en blanding af to farvestoffer (blå) i dens komponenter, bliver ferskvandsgul. Kredit:The American Chemical Society Kovalente organiske materialer med velordnede porøs -
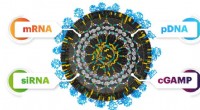 Opdagelse af et universelt system til transport af nukleinsyrer ind i cellerNanopartiklernes alsidighed ligger i, at de kan fungere lige godt for forskellige nukleinsyrer. Dette kan fremskynde lægemiddeludviklingen betydeligt. Kredit:Tomas Bellon / IOCB Prag Forskere fra
Opdagelse af et universelt system til transport af nukleinsyrer ind i cellerNanopartiklernes alsidighed ligger i, at de kan fungere lige godt for forskellige nukleinsyrer. Dette kan fremskynde lægemiddeludviklingen betydeligt. Kredit:Tomas Bellon / IOCB Prag Forskere fra


