Hvorfor opløses ikke i vandet?
* ionisk karakter: CuO er primært en ionisk forbindelse. Ioniske forbindelser opløses generelt godt i polære opløsningsmidler som vand, men kun hvis den energi, der frigøres ved dannelsen af ion-dipol-interaktioner mellem ioner og vandmolekyler, er større end den energi, der kræves for at bryde de ioniske bindinger i det faste stof.
* gitterenergi: Cuo har en relativt høj gitterenergi. Dette betyder, at den elektrostatiske tiltrækning mellem kobber (II) kationer (Cu²⁺) og oxidanioner (O²⁻) i krystalgitteret er stærk. At bryde disse obligationer kræver meget energi.
* Hydratiseringsenergi: Mens Cu²⁺ -ioner kan hydreres af vandmolekyler, er hydratiseringsenergien for Cu²⁺ ikke høj nok til at overvinde CuO's stærke gitterenergi.
* Uopløselighedsprodukt: Opløselighedsproduktkonstanten (KSP) for CuO er meget lav, hvilket indikerer, at meget lidt af det faste opløste vand ved vandløb.
Kortfattet: De stærke ioniske bindinger i CuO og den relativt lave hydratiseringsenergi af Cu²⁺ forhindrer den i at opløse markant i vand.
 Varme artikler
Varme artikler
-
 Mantis rejer perfekt skjoldEn mantis-reje krøller et skjoldlignende segment på halen, kaldet en telson, for at beskytte sig selv mod slag fra en rivaliserende mantis-rejes kraftfulde dactylklub. Kredit:Roy Caldwell/UC Berkeley
Mantis rejer perfekt skjoldEn mantis-reje krøller et skjoldlignende segment på halen, kaldet en telson, for at beskytte sig selv mod slag fra en rivaliserende mantis-rejes kraftfulde dactylklub. Kredit:Roy Caldwell/UC Berkeley -
 Bygger bedre batterier ved at låne fra biologiFigur 1:Struktur af den nyudviklede ioniske krystal. Den vej, hvor ionerne kan rejse, er markeret med gult. Kredit:Osaka University Et forskerhold ved Osaka University har rapporteret et nyt frems
Bygger bedre batterier ved at låne fra biologiFigur 1:Struktur af den nyudviklede ioniske krystal. Den vej, hvor ionerne kan rejse, er markeret med gult. Kredit:Osaka University Et forskerhold ved Osaka University har rapporteret et nyt frems -
 Sjældne jordarter bliver kun vandafvisende, når de bliver ældreOxider af sjældne jordarter (rød/orange) reagerer med gasformige organiske forbindelser fra den omgivende luft og danner carbonater og hydroxider (grå/hvid). Gennem denne reaktion, overfladen udvikler
Sjældne jordarter bliver kun vandafvisende, når de bliver ældreOxider af sjældne jordarter (rød/orange) reagerer med gasformige organiske forbindelser fra den omgivende luft og danner carbonater og hydroxider (grå/hvid). Gennem denne reaktion, overfladen udvikler -
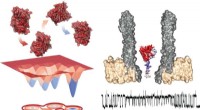 Nanopore afslører formskiftende enzym forbundet med katalyseEnergidiagram over de fire konformere (til venstre) og den eksperimentelle opsætning, der viser nanoporen med det fangede enzym i tværsnit (højre). Under, der er et typisk spor, der viser målinger und
Nanopore afslører formskiftende enzym forbundet med katalyseEnergidiagram over de fire konformere (til venstre) og den eksperimentelle opsætning, der viser nanoporen med det fangede enzym i tværsnit (højre). Under, der er et typisk spor, der viser målinger und
- Hvad observerer du, når kogende vand?
- Hvem opfandt telegrafen?
- Forskeres gennemgribende opdagelse viser, hvordan nyreceller fornyer sig selv
- Videnskabsmæssige ideer med en baseball
- Forskere fanger første gang nogensinde en skjult kvantefase i en 2D-krystal
- Jagten på mikroskopiske lægemidler, der kan spores, mens de bekæmper kræft


