Hvad sker der med partiklerne af fast stof blev til gas?
* Øget energi: Partiklerne i den faste absorberende energi, normalt i form af varme. Denne energi får partiklerne til at vibrere hurtigere.
* Breaking Bonds: Når partiklerne vibrerer mere intenst, holder bindingerne dem sammen i den stive struktur af den faste svækkelse og til sidst går i stykker.
* Øget afstand: Partiklerne får nok energi til at overvinde de attraktive kræfter mellem dem og undslippe fast tilstand. De bevæger sig frit, ligesom gaspartikler, med meget større afstand mellem dem.
* Ændring i tilstand: Partiklerne er nu langt fra hinanden og bevæger sig uafhængigt og udviser egenskaberne ved en gas.
Tænk på det sådan:
Forestil dig en tæt pakket skare af mennesker, der står stille (repræsenterer den solide tilstand). Efterhånden som mængden bliver mere ophidset (energiindgang), begynder folk at bevæge sig mere (øget vibrationer), skubbe hinanden fra hinanden (brud på obligationer), og til sidst bliver de en spredt gruppe, der bevæger sig frit (gasstat).
Her er nogle almindelige eksempler på sublimering:
* Tøris (solid CO2) sublimes direkte i kuldioxidgas ved stuetemperatur.
* frosset vand (is) kan sublimt under kolde, tørre forhold, hvilket fører til frostskader.
* Mothballs langsomt sublim, der frigiver en damp, der afviser møll.
 Varme artikler
Varme artikler
-
 Stanford-forskning kan føre til injicerbare geler, der frigiver medicin over tidKredit:Pixabay/CC0 Public Domain Geler dannes ved at blande polymerer i væsker for at skabe klistrede stoffer, der er nyttige til alt fra at holde hår på plads til at gøre det muligt for kontaktli
Stanford-forskning kan føre til injicerbare geler, der frigiver medicin over tidKredit:Pixabay/CC0 Public Domain Geler dannes ved at blande polymerer i væsker for at skabe klistrede stoffer, der er nyttige til alt fra at holde hår på plads til at gøre det muligt for kontaktli -
 Metal fører til den ønskede konfigurationForskere var i stand til at bestemme det rumlige arrangement af bipyridinmolekyler (grå) på en overflade af nikkel- og oxygenatomer (gul/rød). Rotation ændrer transkonfigurationen (forrest til højre)
Metal fører til den ønskede konfigurationForskere var i stand til at bestemme det rumlige arrangement af bipyridinmolekyler (grå) på en overflade af nikkel- og oxygenatomer (gul/rød). Rotation ændrer transkonfigurationen (forrest til højre) -
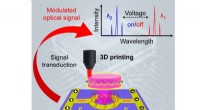 Ny rekord:3-D-printet optisk-elektronisk integrationSkematisk illustration af et integreret elektrisk styret mikrolasermodul til optoelektronisk hybridintegration. Kort, dette modul er designet til at være en termo-responsiv polymerresonator oven på et
Ny rekord:3-D-printet optisk-elektronisk integrationSkematisk illustration af et integreret elektrisk styret mikrolasermodul til optoelektronisk hybridintegration. Kort, dette modul er designet til at være en termo-responsiv polymerresonator oven på et -
 Ny metode til fortolkning af cryo-EM-kort gør det lettere at bestemme proteinstrukturerDaisuke Kihara og Genki Terashi har skabt en ny metode til fortolkning af densitetskort bestemt med kryo-elektronmikroskopi. Kredit:Purdue University foto/John Underwood En ny algoritme gør fortol
Ny metode til fortolkning af cryo-EM-kort gør det lettere at bestemme proteinstrukturerDaisuke Kihara og Genki Terashi har skabt en ny metode til fortolkning af densitetskort bestemt med kryo-elektronmikroskopi. Kredit:Purdue University foto/John Underwood En ny algoritme gør fortol
- Forbrugere af næsehornshorn afslører, hvorfor en lovlig handel alene ikke vil redde næsehorn
- Turboladning af brændselsceller med en multifunktionel katalysator
- Herbert Spencer Gasser
- Nobelpris:Hvorfor klimamodellerer fortjente fysikprisen – de har fået ret igen og
- Hvor lang tid tager det at få bunden af Grand Canyon?
- Mulige fejl i loveksperiment?


