Hvordan bliver et jernatom ferrisk ion?
1. Det grundlæggende
* jernatom: Et jernatom har 26 protoner (positiv ladning), 26 elektroner (negativ ladning) og typisk 30 neutroner. Det er elektrisk neutralt, fordi antallet af protoner og elektroner er ens.
* ferriion: En ferrisk ion (Fe³⁺) er et jernatom, der har mistet tre elektroner. Dette efterlader det med en netto positiv opladning på +3.
2. Processen
Transformationen fra jernatom til ferriskion sker normalt gennem oxidation . Her er en forenklet forklaring:
* Tab af elektroner: Et jernatom mister tre elektroner, typisk til et mere elektronegativt element som ilt. Denne proces kræver energi, der kan komme fra varme, lys eller kemiske reaktioner.
* Dannelse af kationer: Når et atom mister elektroner, bliver det positivt ladet og kaldes en kation. I dette tilfælde bliver jernatomet en ferriion (Fe³⁺).
3. Eksempel:Rust
Et almindeligt eksempel er dannelsen af rust. Når jern udsættes for luft og fugt, opstår følgende reaktion:
* jern (Fe) + ilt (O₂) + vand (H₂O) → Jernoxid (Fe₂o₃) (Rust) + Hydrogen (H₂)
I denne reaktion mister jernatomer elektroner til iltatomer og danner jernoxid (RUST) og jernioner (Fe³⁺).
4. Kemisk notation
Den kemiske notation til processen kan skrives som:
* Fe → Fe³⁺ + 3e⁻
Dette viser, at et jernatom (Fe) mister tre elektroner (E⁻) for at blive en ferriskion (Fe³⁺).
Kortfattet:
Et jernatom bliver en ferriskion ved at miste tre elektroner gennem en proces kaldet oxidation. Dette forekommer typisk i nærvær af ilt og vand, som i dannelsen af rust.
 Varme artikler
Varme artikler
-
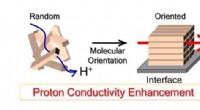 Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri
Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri -
 PolymerkraftpotentialeKredit:Agency for Science, Teknologi og forskning (A*STAR), Singapore Mantraet reducere, genbruge, genbrug er mere og mere relevant. Hvert år, enorme mængder energi, der kunne opsamles og genbruge
PolymerkraftpotentialeKredit:Agency for Science, Teknologi og forskning (A*STAR), Singapore Mantraet reducere, genbruge, genbrug er mere og mere relevant. Hvert år, enorme mængder energi, der kunne opsamles og genbruge -
 Succesfuld syntese af nanomateriale, der forbedrer katalysatorens effektivitet(Venstre mod højre) Dr. Md Shahriar Hossain, Prof Yusuke Yamauchi og Dr. Katy Wood ved Quokka-instrumentet. Kredit:Australian Nuclear Science and Technology Organisation (ANSTO) Et stort internati
Succesfuld syntese af nanomateriale, der forbedrer katalysatorens effektivitet(Venstre mod højre) Dr. Md Shahriar Hossain, Prof Yusuke Yamauchi og Dr. Katy Wood ved Quokka-instrumentet. Kredit:Australian Nuclear Science and Technology Organisation (ANSTO) Et stort internati -
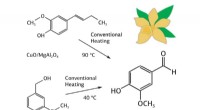 Kemiker skaber billige katalysatorer til produktion af vanillinKredit:RUDN University En kemiker fra RUDN University har skabt billige og effektive katalysatorer til produktion af vanillin ved hjælp af spinel -nanopartikler med kobberoxid -nanopartikler. Hydr
Kemiker skaber billige katalysatorer til produktion af vanillinKredit:RUDN University En kemiker fra RUDN University har skabt billige og effektive katalysatorer til produktion af vanillin ved hjælp af spinel -nanopartikler med kobberoxid -nanopartikler. Hydr
- Afslører denne dinosaurkirkegård deres sidste dag på jorden? En ekspert udforsker beviserne
- Sovetid til New Horizons:Rumfartøj går i dvale
- Hvad er den relative størrelse på 3 subatomære partikler?
- Ved hvilken temperatur bliver ilt en væske?
- Hvad ville der ske, hvis du forbrændte flere fossile brændstoffer?
- Biokemikere undersøger transporten af store proteiner gennem bakterielle cellemembraner


