Bidrager elektronerne af et atom til masseatom?
Her er hvorfor:
* masse af partikler:
* Protoner: 1 Atommasseenhed (AMU)
* neutroner: 1 amu
* Elektroner: 0,00054858 AMU (ca. 1/1836 af en AMU)
* Antal partikler: Atomer har typisk et lige antal protoner og elektroner. Antallet af neutroner kan variere, hvilket fører til isotoper.
Derfor, mens elektroner bidrager til atomets masse, er deres bidrag ubetydelig sammenlignet med protoner og neutroner. Dette er grunden til, at atommasse ofte tilnærmes som summen af protoner og neutroner og ignorerer elektronerne.
Imidlertid bliver elektronernes masse i nogle tilfælde betydelig:
* Målinger med høj præcision: I meget præcise målinger af atommasse skal bidraget fra elektroner overvejes.
* Fysik med høj energi: I fysik med høj energi, hvor partikler accelereres til nær lysets hastighed, kan den relativistiske masseforøgelse på grund af elektronernes hastighed blive betydelig.
Samlet set, mens elektroner bidrager til en atoms masse, er deres bidrag normalt lille og ignoreres ofte til praktiske formål.
Sidste artikelHvad er de fysiske egenskaber ved benzanilid?
Næste artikelHvad sker der i en synteseaktion?
 Varme artikler
Varme artikler
-
 Sød succes:Nyt enzymatisk biosystem høster potentialet i sukkermaltosenKredit:Unsplash/CC0 Public Domain Mikroorganismefri enzymbaserede reaktionssystemer bruges nu til produktion af brint, bioelektricitet og nyttige biokemikalier. I disse biosystemer nedbrydes råmate
Sød succes:Nyt enzymatisk biosystem høster potentialet i sukkermaltosenKredit:Unsplash/CC0 Public Domain Mikroorganismefri enzymbaserede reaktionssystemer bruges nu til produktion af brint, bioelektricitet og nyttige biokemikalier. I disse biosystemer nedbrydes råmate -
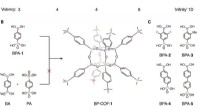 Ny kovalent organisk ramme, der bruger bor og fosfor, giver mulighed for bedre tilslutningHøjere valens i COFer og syntetisk strategi for polycubaner. (A) Bygningsenheder med valens 3 og 4 bruges i øjeblikket i design og syntese af 3D COFer; terninger med valens på 8 og uendelige 1D-stænge
Ny kovalent organisk ramme, der bruger bor og fosfor, giver mulighed for bedre tilslutningHøjere valens i COFer og syntetisk strategi for polycubaner. (A) Bygningsenheder med valens 3 og 4 bruges i øjeblikket i design og syntese af 3D COFer; terninger med valens på 8 og uendelige 1D-stænge -
 Glaslignende træ isolerer varme, er hård, blokerer UV og har trækornet mønsterIngeniører ved University of Maryland designede et gennemsigtigt loft lavet af træ, der fremhæver det naturlige trækornmønster. Kredit:A.James Clark School of Engineering, University of Maryland B
Glaslignende træ isolerer varme, er hård, blokerer UV og har trækornet mønsterIngeniører ved University of Maryland designede et gennemsigtigt loft lavet af træ, der fremhæver det naturlige trækornmønster. Kredit:A.James Clark School of Engineering, University of Maryland B -
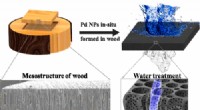 Træfilter fjerner giftigt farvestof fra vandetKredit:ACS Ingeniører ved University of Maryland har udviklet en ny anvendelse af træ:at filtrere vand. Liangbing Hu fra Energy Research Center og hans kolleger tilføjede nanopartikler til træ, br
Træfilter fjerner giftigt farvestof fra vandetKredit:ACS Ingeniører ved University of Maryland har udviklet en ny anvendelse af træ:at filtrere vand. Liangbing Hu fra Energy Research Center og hans kolleger tilføjede nanopartikler til træ, br
- Hvad sker der, når flyet går hurtigere end hastighedslyd?
- Hvordan lasere og 2D-materialer kunne løse verdens plastikproblem
- Hvor langt væk er den nærmeste stjerne på Jorden eksklusive sol?
- Hvordan ændres de forvitrede klipper til frugtbar jord?
- Hvor stiger månen i forhold til Horizon?
- Er moset zink en elementforbindelse eller blanding?


