Hvad sker der i en synteseaktion?
Tænk på det som at opbygge en LEGO -struktur. Du starter med individuelle mursten (reaktanter) og sætter dem sammen for at skabe en større, mere kompliceret model (produkt).
Her er en sammenbrud:
* reaktanter: De startstoffer, der er kombineret.
* Produkt: Det nye stof dannet fra reaktionen.
* Kemisk ligning: Den symbolske repræsentation af reaktionen, normalt skrevet som: reaktant 1 + reaktant 2 → Produkt
Eksempler på synteseaktioner:
* Dannelse af vand: Hydrogengas (H₂) reagerer med iltgas (O₂) for at danne vand (H₂O).
* Dannelse af natriumchlorid: Natriummetal (NA) reagerer med chlorgas (CL₂) for at danne natriumchlorid (NaCl), bordsalt.
* forbrænding af brændstoffer: Et brændstof (som metan, CH₄) reagerer med ilt (O₂) for at producere kuldioxid (CO₂) og vand (H₂O).
Nøgleegenskaber ved synteseaktioner:
* Forøgelse i kompleksitet: Produktet er mere kompliceret end reaktanterne.
* Energiændring: Disse reaktioner kan være eksoterme (frigivelse af varme) eller endotermisk (absorberende varme).
* Dannelse af nye obligationer: Nye kemiske bindinger dannes mellem de reagerende atomer.
At forstå synteseaktioner er afgørende for at forstå grundlæggende kemi og dannelse af nye forbindelser. De er grundlæggende for forskellige processer i naturen og industrien.
 Varme artikler
Varme artikler
-
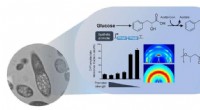 Et-trins produktion af aromatiske polyestere af E. coli-stammerBiosyntese af aromatiske polyestere ved metabolisk manipuleret E coli .Dette skematiske diagram viser den overordnede konceptualisering af, hvordan metabolisk manipuleret E coli fremstillet aromat
Et-trins produktion af aromatiske polyestere af E. coli-stammerBiosyntese af aromatiske polyestere ved metabolisk manipuleret E coli .Dette skematiske diagram viser den overordnede konceptualisering af, hvordan metabolisk manipuleret E coli fremstillet aromat -
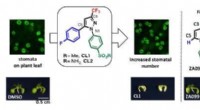 Flere mund kan fodres ved at øge antallet af plantens porerForbindelser, der øger antallet af stomata på planter. Kredit:Nagoya University Miljøundersøgelser har vist, at 40% af det atmosfæriske kuldioxid (CO2) passerer hvert år gennem plantemateriale. De
Flere mund kan fodres ved at øge antallet af plantens porerForbindelser, der øger antallet af stomata på planter. Kredit:Nagoya University Miljøundersøgelser har vist, at 40% af det atmosfæriske kuldioxid (CO2) passerer hvert år gennem plantemateriale. De -
 Forskere bruger 3D-tryk til at skabe metalliske glaslegeringer i løs vægtCylinderen vist her er en amorf jernlegering, eller metallisk glas, lavet ved hjælp af en additiv fremstillingsteknik. Kredit:Zaynab Mahbooba Forskere har nu demonstreret evnen til at skabe amorft
Forskere bruger 3D-tryk til at skabe metalliske glaslegeringer i løs vægtCylinderen vist her er en amorf jernlegering, eller metallisk glas, lavet ved hjælp af en additiv fremstillingsteknik. Kredit:Zaynab Mahbooba Forskere har nu demonstreret evnen til at skabe amorft -
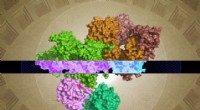 Forskere identificerer molekylær struktur af GATOR1 -proteinkomplekset, der regulerer cellulære væ…Den cryo-EM-genererede GATOR1-struktur kan give indsigt i dens funktion. Kredit:Steven Lee/Whitehead Institute Et team af forskere fra Whitehead Institute og Howard Hughes Medical Institute har af
Forskere identificerer molekylær struktur af GATOR1 -proteinkomplekset, der regulerer cellulære væ…Den cryo-EM-genererede GATOR1-struktur kan give indsigt i dens funktion. Kredit:Steven Lee/Whitehead Institute Et team af forskere fra Whitehead Institute og Howard Hughes Medical Institute har af
- Hvilket element fortsætter med at henfalde, indtil de endelig bliver stabile?
- Jordens søer udleder mindre metan end tidligere antaget
- Middelhavs vingårde er i et klima -hotspot. Klimatologer hjælper dem med at tilpasse sig
- Hvordan får planter protein?
- Hvor meget energi kan vind levere?
- Pulsar jackpot afslører kugleformede klyngers indre struktur


