Hvilke egenskaber deler gasser og væsker?
1. Fluiditet: Både gasser og væsker kan flyde og tage formen på deres beholder. Dette skyldes, at partiklerne i begge stofstater har evnen til at bevæge sig forbi hinanden frit.
2. Kompressibilitet: Både gasser og væsker kan komprimeres, hvilket betyder, at deres volumen kan reduceres ved at påføre tryk. Dette skyldes, at partiklerne i begge stater ikke er fastgjort i en stiv struktur.
3. Termisk ekspansion: Både gasser og væsker ekspanderer, når de opvarmes. Dette skyldes, at den øgede termiske energi får partiklerne til at bevæge sig hurtigere og sprede sig.
4. Diffusion: Både gasser og væsker udviser diffusion, som er bevægelsen af partikler fra et område med høj koncentration til et område med lav koncentration. Dette forekommer på grund af partiklernes tilfældige bevægelse.
5. Fravær af fast form: Både gasser og væsker har ikke en fast form. De tager formen på deres container.
6. Relativ densitet: Mens gasser generelt er mindre tætte end væsker, kan de stadig dele lignende densiteter afhængigt af de involverede specifikke stoffer.
7. Evne til at opløse stoffer: Både gasser og væsker kan opløse andre stoffer, selvom gasser typisk har en lavere opløselighed end væsker.
8. Evne til at overføre tryk: Både gasser og væsker kan transmittere tryk lige i alle retninger. Dette skyldes partiklernes evne til at bevæge sig og interagere med hinanden.
Det er dog vigtigt at bemærke, at der også er centrale forskelle mellem gasser og væsker. Disse forskelle stammer fra den større bevægelsesfrihed og de svagere intermolekylære kræfter mellem gasmolekyler sammenlignet med væsker.
Sidste artikelUdseendet af faste metaller kan beskrives som?
Næste artikelSammenlign og kontrast egenskaberne ved væskesolit?
 Varme artikler
Varme artikler
-
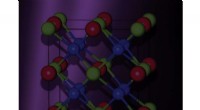 Fremstilling af nye katalysatorer af unikke metalliske legeringerTsai og hans kolleger tror på materialeinformatik, som bruger big data til at opdage nye materialer, kunne være særligt relevant for opdagelsen af nye katalysatorer fra Heusler-legeringer på grund a
Fremstilling af nye katalysatorer af unikke metalliske legeringerTsai og hans kolleger tror på materialeinformatik, som bruger big data til at opdage nye materialer, kunne være særligt relevant for opdagelsen af nye katalysatorer fra Heusler-legeringer på grund a -
 Lab afslører ny virkningsmekanisme mod SARS-CoV-2 af antiviralt lægemiddel remdesivir(Top) Den virale polymerase (blå oval) inkorporerer remdesivir (rød) i RNA-primerstrengen (grønne bobler) modsat uridin i skabelonen (gule/klare bobler). Et sammenstød mellem remdesivir og aminosyren
Lab afslører ny virkningsmekanisme mod SARS-CoV-2 af antiviralt lægemiddel remdesivir(Top) Den virale polymerase (blå oval) inkorporerer remdesivir (rød) i RNA-primerstrengen (grønne bobler) modsat uridin i skabelonen (gule/klare bobler). Et sammenstød mellem remdesivir og aminosyren -
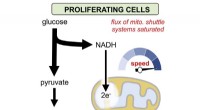 Sukkermetabolisme er overraskende konventionelt ved kræftGrafisk abstrakt. Kredit:Molecular Cell (2022). DOI:10.1016/j.molcel.2022.07.007 I over et århundrede har kræftcellernes stofskifte været betragtet som noget af et paradoks. Nyt arbejde fra forsker
Sukkermetabolisme er overraskende konventionelt ved kræftGrafisk abstrakt. Kredit:Molecular Cell (2022). DOI:10.1016/j.molcel.2022.07.007 I over et århundrede har kræftcellernes stofskifte været betragtet som noget af et paradoks. Nyt arbejde fra forsker -
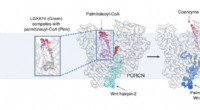 Nye cryo-EM-billeder kaster lys over Wnt-signaleringCryo-EM afslører, hvordan Wnt, et nøglesignalmolekyle for menneskelig udvikling og kræft, modificeres af et enzym ved navn PORCN. Kredit:UT Southwestern Medical Center Ved hjælp af UT Southwesterns
Nye cryo-EM-billeder kaster lys over Wnt-signaleringCryo-EM afslører, hvordan Wnt, et nøglesignalmolekyle for menneskelig udvikling og kræft, modificeres af et enzym ved navn PORCN. Kredit:UT Southwestern Medical Center Ved hjælp af UT Southwesterns
- Hvad er afkom til en guillimot?
- Forskere viser ophidsede elektroner, der retter det skæve gitter af perovskit nanokrystaller
- Hvordan bevæger lyset sig fra solen til jorden?
- Hvilken type sedimentære klipper danner sammenbrudplanter?
- Specifikationssårbarhed på enheder, der taler Bluetooth, behandles
- Hvilke aktiviteter laver folk normalt om foråret?


