Hvorfor er gasser bedre isolatorer end væsker?
* lavere densitet: Gasser har meget lavere densitet end væsker. Dette betyder, at der er færre molekyler pr. Enhedsvolumen i en gas, hvilket fører til færre kollisioner og mindre energioverførsel gennem ledning.
* Større afstande mellem molekyler: I gasser er molekyler langt længere fra hinanden end i væsker. Denne øgede afstand gør det sværere for energi at overføre gennem kollisioner mellem molekyler.
* mindre effektiv energioverførsel: Kollisioner mellem gasmolekyler er mindre hyppige og mindre energiske sammenlignet med kollisioner i væsker. Dette reducerer den hastighed, hvormed varme kan overføres gennem ledning.
Det er dog vigtigt at bemærke, at nogle gasser er bedre isolatorer end andre. Her er hvorfor:
* molekylær kompleksitet: Mere komplekse gasmolekyler (som dem med mange atomer) kan absorbere mere energi og overføre det mindre effektivt.
* Polaritet: Polære molekyler kan interagere stærkere med hinanden, hvilket fører til lidt bedre varmeoverførsel sammenlignet med ikke-polære gasser.
Eksempler:
* luft: En god isolator, primært på grund af dens lave densitet og den for det meste ikke-polære karakter af dens molekyler.
* Argon: En endnu bedre isolator end luft på grund af dens ikke-polære karakter og dens større atomstørrelse.
* Vand: En bedre leder af varme end luft, primært på grund af dens høje densitet og dens polære karakter.
Kortfattet: Mens både gasser og væsker kan fungere som isolatorer, udmærker gasser generelt på grund af deres lave densitet, store molekylære afstand og mindre hyppige kollisioner, hvilket gør dem mindre effektive til at overføre varme.
Sidste artikelKan andre materialer ændre sig til gas og bagvæske?
Næste artikelHvad er den molære masse af Na2S04?
 Varme artikler
Varme artikler
-
 Fysiker skaber N95-type åndedrætsværn ved hjælp af en bomuldsmaskineKredit:Pixabay/CC0 Public Domain Mahesh Bandi, en fysiker med den ikke-lineære og ikke-ligevægtsfysikenhed, OIST Graduate University, Onna, Okinawa, har fundet en måde at fremstille N95-type respi
Fysiker skaber N95-type åndedrætsværn ved hjælp af en bomuldsmaskineKredit:Pixabay/CC0 Public Domain Mahesh Bandi, en fysiker med den ikke-lineære og ikke-ligevægtsfysikenhed, OIST Graduate University, Onna, Okinawa, har fundet en måde at fremstille N95-type respi -
 Maskinlæringshjælpemidler i materialedesignForskere udviklede en maskinlæringsalgoritme til at forudsige 3D molekylær krystaldensitet ud fra 2D kemiske strukturer. Kredit:Lawrence Livermore National Laboratory Et langvarigt mål af kemikere
Maskinlæringshjælpemidler i materialedesignForskere udviklede en maskinlæringsalgoritme til at forudsige 3D molekylær krystaldensitet ud fra 2D kemiske strukturer. Kredit:Lawrence Livermore National Laboratory Et langvarigt mål af kemikere -
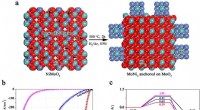 Ny metode til syntese af molekylært hydrogen sætter benchmark for platinfri elektrokatalysatorerFigur. a) Syntetisk skema af MoNi4 elektrokatalysator understøttet af MoO2 kuboiderne på nikkelskum; b) polarisationskurver for MoNi4 elektrokatalysatoren understøttet af MoO2 kuboiderne, rene Ni nano
Ny metode til syntese af molekylært hydrogen sætter benchmark for platinfri elektrokatalysatorerFigur. a) Syntetisk skema af MoNi4 elektrokatalysator understøttet af MoO2 kuboiderne på nikkelskum; b) polarisationskurver for MoNi4 elektrokatalysatoren understøttet af MoO2 kuboiderne, rene Ni nano -
 Ingeniører introducerer en ny tilgang til genanvendelse af plastEPFL-ingeniører introducerer en ny tilgang til genanvendelse af plast. Kredit:Alain Herzog / EPFL 2021 Hvert menneske bruger, gennemsnitlig, 30 kg plastik om året. I betragtning af at den globale
Ingeniører introducerer en ny tilgang til genanvendelse af plastEPFL-ingeniører introducerer en ny tilgang til genanvendelse af plast. Kredit:Alain Herzog / EPFL 2021 Hvert menneske bruger, gennemsnitlig, 30 kg plastik om året. I betragtning af at den globale
- Er jernchlorid og natriumhydroxid en fysisk eller kemisk ændring?
- Nye beviser viser, at nuværende politikker ikke virker for at stoppe plastikforurening
- De første blomster udviklede sig før bier – så hvordan blev de så blændende?
- Kuldioxidniveauer lavere end antaget i løbet af super drivhusperioden
- Er helium tæt eller mindre end vand?
- Hvilken faktor har den største indflydelse på forvitringshastigheden på jordoverfladen?


