Hvilket volumen gas produceres af 4 gram sukker?
* Hvilken reaktion? Sukker producerer ikke bare spontant gas. Det skal gennemgå en kemisk reaktion. Almindelige reaktioner, der involverer sukker, inkluderer:
* forbrænding: Brændende sukker i nærvær af ilt producerer kuldioxid (CO2) og vanddamp (H2O).
* gæring: Gær kan opdele sukker i ethanol (C2H5OH) og kuldioxid.
* Betingelser: Mængden af produceret gas afhænger af forholdene, herunder:
* Temperatur: Højere temperaturer fører til større gasvolumen.
* tryk: Højere tryk reducerer gasvolumen.
For at beregne gasvolumen skal du vide:
1. Den specifikke reaktion: Hvad er den kemiske reaktion, der forekommer?
2. reaktionsbetingelserne: Temperatur og tryk.
Eksempel:
Lad os sige, at vi brænder 4 gram sukker (C12H22O11) helt i nærvær af ilt ved 25 ° C og 1 atm -tryk (standardbetingelser). Den afbalancerede kemiske ligning er:
C12H22O11 + 12O2 → 12CO2 + 11H2O
Fra dette kan vi beregne:
1. mol af sukker: 4 g / 342,3 g / mol =0,0117 mol (molmasse sukker)
2. mol produceret CO2: 0,0117 mol * 12 =0,14 mol (12 mol CO2 produceres pr. Mol sukker)
3. Volumen af CO2 på STP: 0,14 mol * 22,4 L/mol =3,14 L (ved hjælp af den ideelle gaslov ved standardtemperatur og tryk)
Derfor ville forbrænding af 4 gram sukker ved standardforhold producere cirka 3,14 liter CO2.
Hvis du giver den specifikke reaktion og betingelser, kan jeg hjælpe dig med at beregne mængden af produceret gas.
 Varme artikler
Varme artikler
-
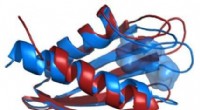 Røntgenøjne kigger dybere ind i dødbringende patogenSammenligning af strukturerne af Flpp3-proteinrygraden som afledt af en røntgenfri elektronlaser (rød) og fra NMR (blå) afslører et indre hulrum, der er unikt for NMR-strukturen og antyder derfor eksi
Røntgenøjne kigger dybere ind i dødbringende patogenSammenligning af strukturerne af Flpp3-proteinrygraden som afledt af en røntgenfri elektronlaser (rød) og fra NMR (blå) afslører et indre hulrum, der er unikt for NMR-strukturen og antyder derfor eksi -
 Bakteriebaseret beton giver klimafordeleBeton genererer enorme mængder drivhusgasser. Derfor ser forskere på at producere mere miljøvenlige former for dette vigtige byggemateriale. Kredit:Shutterstock Byggebranchen udleder enorme mængde
Bakteriebaseret beton giver klimafordeleBeton genererer enorme mængder drivhusgasser. Derfor ser forskere på at producere mere miljøvenlige former for dette vigtige byggemateriale. Kredit:Shutterstock Byggebranchen udleder enorme mængde -
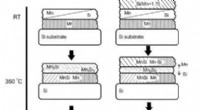 Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc
Fysikere overvåger dannelsen af film med højere mangansilicidSkematisk illustration af synteseproceduren til venstre:Mn17Si30 og højre Mn4Si7 -prøve. Kredit:Ivan Tarasov Et team fra Kirensky Institute of Physics (Siberian Branch of the Russian Academy of Sc -
 Lad solen skinne ind:Selvrensende membran under synlig lysbehandlingDen hydrofile fotokatalytiske membran udviste fremragende antimikrobiel aktivitet under synligt lys, og den anti-biobegroningsegenskab muliggjorde en fuldstændig fluxgenvinding af membranen i gentagne
Lad solen skinne ind:Selvrensende membran under synlig lysbehandlingDen hydrofile fotokatalytiske membran udviste fremragende antimikrobiel aktivitet under synligt lys, og den anti-biobegroningsegenskab muliggjorde en fuldstændig fluxgenvinding af membranen i gentagne
- Forbedring af elektrogenereret kemiluminescens af et iridiumkompleks
- Forskning:Udfordringer unge afrikanske migranter står over for, når de tilpasser sig livet i Austr…
- Præcisionskontrol af superledning i atomlag ved hjælp af magnetiske molekyler
- Hvad er de vigtigste fysiske træk ved Guyana?
- Hvilken planet er blå med svage ringe?
- Hvorfor er faste stoffer stive og ikke komprimeret mærkbart selv ved højt tryk?


